8.5 – Configuration des Électrons dans les Atomes et Caractéristiques
Un électron dans un atome est entièrement décrit par quatre nombres quantiques : n, l, ml et ms. Les trois premiers nombres quantiques définissent l’orbitale et le quatrième nombre quantique décrit la propriété intrinsèque de l’électron appelée spin. Le physicien autrichien Wolfgang Pauli a formulé un principe général qui donne la dernière information dont nous avons besoin pour comprendre le comportement général des électrons dans les atomes. Le principe d'exclusion de Pauli peut être formulé comme suit: Deux électrons d’un même atome ne peuvent pas avoir exactement le même ensemble des quatre nombres quantiques. Cela signifie que les électrons peuvent partager la même orbitale (le même ensemble de nombres quantiques n, l et ml), mais seulement si leurs nombres quantiques de spin ms ont des valeurs différentes. Comme le nombre quantique de spin ne peut avoir que deux valeurs (
), pas plus de deux électrons ne peuvent occuper la même orbitale (et si deux électrons sont situés dans la même orbitale, ils doivent avoir des spins opposés). Par conséquent, toute orbitale atomique ne peut être peuplée que par zéro, un ou deux électrons.
Les propriétés et la signification des nombres quantiques des électrons dans les atomes sont brièvement résumées dans le tableau suivant.
|
Les nombres quantiques, leurs propriétés et leur signification |
|||
|
Nom |
Symbole |
Valeurs autorisées |
Signification physique |
|
nombre quantique principal |
n |
1, 2, 3, 4, …. |
la valeur générale de l’énergie pour un électron dans l’orbite |
|
le moment angulaire ou le nombre quantique azimutal |
l |
0 ≤ l ≤ n – 1 |
la forme de l’orbitale |
|
nombre quantique magnétique |
ml |
– l ≤ ml ≤ l |
Nombre et orientation des orbitales dans la sous-couche |
|
nombre quantique de spin |
ms |
12
, -12
|
direction de la « rotation » quantique intrinsèque de l’électron |
Exemple 8.5.1 – Travailler avec des couches et des sous-couches
Indiquez le nombre de sous-couches, le nombre d’orbitales dans chaque sous-couche, et les valeurs de l et ml pour les orbitales dans la couche n = 4 d’un atome.
Solution
Pour n = 4, l peut prendre les valeurs 0, 1, 2 et 3. On trouve donc des sous-couches s, p, d et f dans la ciuche n = 4 d’un atome. Pour l = 0 (la sous-couche s), ml ne peut être que 0. Ainsi, il n’existe qu’une seule orbitale 4s. Pour l = 1 (orbitales de type p), m peut prendre les valeurs -1, 0, +1, on trouve donc trois orbitales 4p. Pour l = 2 (orbitales de type d), ml peut avoir les valeurs -2, -1, 0, +1, +2, nous avons donc cinq orbitales 4d. Lorsque l = 3 (orbitales de type f), ml peut avoir des valeurs de -3, -2, -1, 0, +1, +2, +3, et nous pouvons avoir sept orbitales 4f. Ainsi, nous trouvons un total de 16 orbitales dans la couche n = 4 d’un atome.
Vérifiez votre apprentissage 8.5.1 – Travailler avec des couches et des sous-couches
Identifiez la sous-couche dans laquelle se trouvent les électrons ayant les nombres quantiques suivants: (a) n = 3, l = 1; (b) n = 5, l = 3; (c) n = 2, l = 0.
Réponse
(a) 3p (b) 5f (c) 2s
Exemple 8.5.2 – Nombre maximal d’électrons
Calculez le nombre maximal d’électrons qui peuvent occuper une couche avec (a) n = 2, (b) n = 5, et (c) n comme variable. Notez que vous ne regardez que les orbitales avec la valeur n spécifiée, et non celles à des énergies inférieures.
Solution
(a) Lorsque n = 2, il y a quatre orbitales (une seule orbitale 2s, et trois orbitales étiquetées 2p). Ces quatre orbitales peuvent contenir huit électrons.
(b) Lorsque n = 5, il y a cinq sous-couches d’orbitales que nous devons additionner:
1 orbitale étiquetée 5s
3 orbitales étiquetées 5p
5 orbitales étiquetées 5d
7 orbitales étiquetées 5f
+9 orbitales étiquetées 5g
25 orbitales totale
Là encore, chaque orbitale contient deux électrons, ce qui signifie que 50 électrons peuvent se trouver dans cette couche.
(c) Le nombre d’orbitales dans une couche n sera égal à n2. Il peut y avoir jusqu’à deux électrons dans chaque orbitale, le nombre maximal d’électrons est donc de 2 × n2.
Vérifiez votre apprentissage 8.5.2 – Nombre maximal d’électrons
Si une couche contient un maximum de 32 électrons, quel est le nombre quantique principal, n?
Réponse
n = 4
Exemple 8.5.3 – Travailler avec des nombres quantiques
Complétez le tableau suivant pour les orbitales atomiques:
|
Orbitale |
n |
l |
ml dégénérescence |
Nœuds radiaux (no.) |
|
4f |
|
|
|
|
|
|
4 |
1 |
|
|
|
|
7 |
|
7 |
3 |
|
5d |
|
|
|
|
Solution
Le tableau peut être complété en utilisant les règles suivantes:
La désignation orbitale est nl, où l = 0, 1, 2, 3, 4, 5, … correspond à la séquence de lettres s, p, d, f, g, h, …,
La dégénérescence ml est le nombre d’orbitales dans une sous-couche l, et donc 2l + 1 (il y a une orbitale s, trois orbitales p, cinq orbitales d, sept orbitales f, et ainsi de suite).
Le nombre de nœuds radiaux est égal à n – l – 1.
|
Orbitale |
n |
l |
ml dégénérescence |
Nœuds radiaux (no.) |
|
4f |
4 |
3 |
7 |
0 |
|
4p |
4 |
1 |
3 |
2 |
|
7f |
7 |
3 |
7 |
3 |
|
5d |
5 |
2 |
5 |
2 |
Vérifiez votre apprentissage 8.5.3 – Travailler avec des nombres quantiques
Combien d’orbitales ont l = 2 et n = 3?
Réponse
Les cinq orbitales 3d dégénérées
Énergies des orbitales et structure atomique
L’énergie des orbitales atomiques augmente lorsque le nombre quantique principal, n, augmente. Dans tout atome comportant deux électrons ou plus, la répulsion entre les électrons fait que les énergies des sous-couches ayant différentes valeurs de l diffèrent, de sorte que l’énergie des orbitales augmente à l’intérieur d’une couche dans l’ordre s < p < d < f. La Figure 8.5.1. illustre la relation entre ces deux tendances à l’augmentation de l’énergie. L’orbitale 1s, en bas du diagramme, est l’orbitale dont les électrons ont la plus faible énergie. L’énergie augmente à mesure que l’on passe aux orbitales 2s, puis 2p, 3s et 3p, ce qui montre que la valeur croissante de n a plus d’influence sur l’énergie que la valeur croissante de l pour les petits atomes. Cependant, ce schéma ne s’applique pas aux atomes plus grands. L’orbitale 3d est plus énergétique que l’orbitale 4s. De tels chevauchements continuent à se produire fréquemment à mesure que l’on monte dans le tableau.
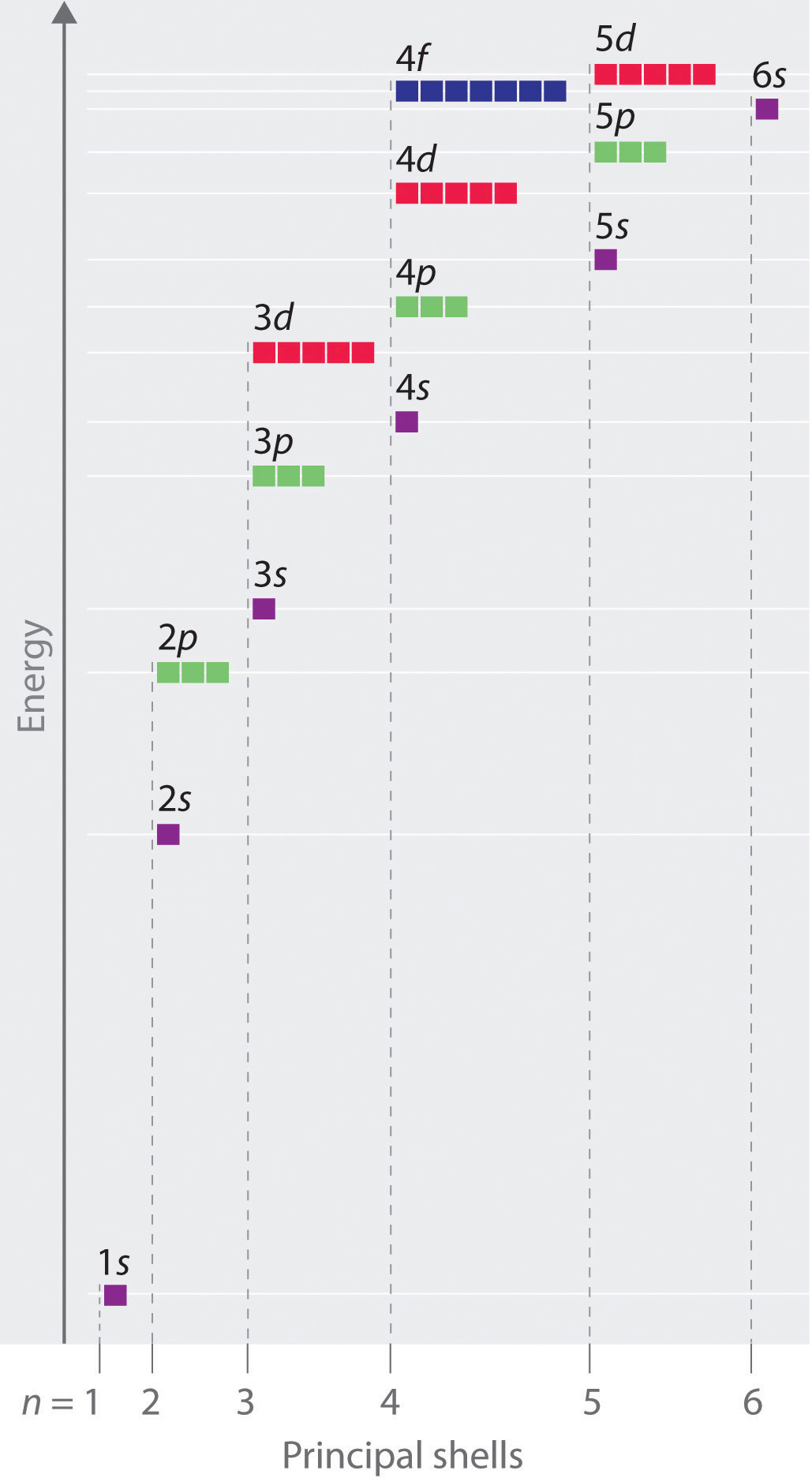
Figure 8.5.1. Diagramme énergétique montrant les niveaux d’énergie relatifs approximatifs des orbitales atomiques dans un atome comportant deux électrons ou plus.
Les électrons des atomes successifs du tableau périodique ont tendance à remplir d’abord les orbitales à faible énergie. Ainsi, de nombreux élèves trouvent déroutant que, par exemple, les orbitales 5p se remplissent immédiatement après les 4d et immédiatement avant les 6s. L’ordre de remplissage est basé sur des résultats expérimentaux observés et a été confirmé par des calculs théoriques. Lorsque le nombre quantique principal, n, augmente, la taille de l’orbitale augmente et les électrons passent plus de temps loin du noyau. Ainsi, l’attraction vers le noyau est plus faible et l’énergie associée à l’orbitale est plus élevée (moins stabilisée). Mais ce n’est pas le seul effet à prendre en compte. À l’intérieur de chaque couche, au fur et à mesure que la valeur de l augmente, les électrons sont moins pénétrants (ce qui signifie qu’il y a moins de densité électronique à proximité du noyau), dans l’ordre s > p > d > f. Les électrons qui sont plus proches du noyau repoussent légèrement les électrons qui sont plus éloignés, ce qui compense légèrement les attractions électron-noyau plus dominantes (rappelons que tous les électrons ont des charges -1, mais que les noyaux ont des charges +Z). Ce phénomène est appelé blindage et sera abordé plus en détail dans la section suivante. Les électrons des orbitales qui subissent un blindage plus important sont moins stabilisés et ont donc une énergie plus élevée. Pour les petites orbitales (1s à 3p), l’augmentation de l’énergie due à n est plus importante que celle due à l; cependant, pour les orbitales plus grandes, les deux tendances sont comparables et ne peuvent pas être simplement prédites. Nous discuterons des méthodes permettant de se souvenir de l’ordre observé.
La disposition des électrons dans les orbitales d’un atome est appelée configuration électronique de l’atome. Nous décrivons une configuration électronique avec un symbole qui contient trois pièces d’information (Figure 8.5.2.):
Le numéro de la couche quantique principale, n,
La lettre qui désigne le type d’orbitale (la sous-couche, l), et
Un nombre en exposant qui désigne le nombre d’électrons dans cette sous-couche particulière.
Par exemple, la notation 2p4 (lire « deux-p-quatre« ) indique quatre électrons dans une sous-couche p (l = 1) avec un nombre quantique principal (n) de 2. La notation 3d8 (lire « trois-d-huit« ) indique huit électrons dans la sous-couche d (c’est-à-dire l = 2) de la couche principale pour laquelle n = 3.
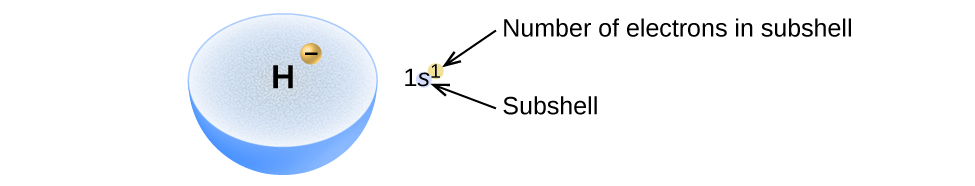
Figure 8.5.2. Le diagramme d’une configuration électronique précise la sous-couche (valeur n et l, avec symbole lettre) et le nombre d’électrons en exposant.
Le principe d’Aufbau
Pour déterminer la configuration électronique d’un atome particulier, nous pouvons « construire » les structures dans l’ordre des numéros atomiques. En commençant par l’hydrogène, et en continuant à travers les périodes du tableau périodique, nous ajoutons un proton à la fois au noyau et un électron à la sous-couche appropriée jusqu’à ce que nous ayons décrit les configurations électroniques de tous les éléments. Cette procédure est appelée le principe d’Aufbau, du mot allemand Aufbau (« construire »). Chaque électron ajouté occupe la sous-couche de plus basse énergie disponible (dans l’ordre indiqué à la Figure 8.5.1.), sous réserve des limitations imposées par les nombres quantiques autorisés selon le principe d’exclusion de Pauli. Les électrons ne pénètrent dans les sous-couches d’énergie supérieure que lorsque les sous-couches d’énergie inférieures ont été remplies à pleine capacité. La Figure 8.5.3. illustre la manière traditionnelle de se souvenir de l’ordre de remplissage des orbitales atomiques. Comme la disposition du tableau périodique est basée sur les configurations électroniques, la Figure 8.5.4. fournit une méthode alternative pour déterminer la configuration électronique. L’ordre de remplissage commence simplement à l’hydrogène et inclut chaque sous-couche au fur et à mesure que l’on progresse dans l’ordre Z croissant. Par exemple, après avoir rempli le bloc 3p jusqu’à Ar, nous voyons que l’orbitale sera 4s (K, Ca), suivie des orbitales 3d.
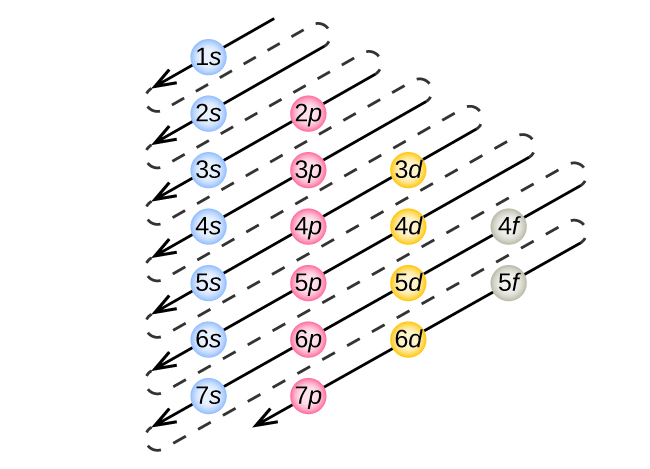
Figure 8.5.3. La flèche traverse chaque sous-couche dans l’ordre de remplissage approprié pour les configurations électroniques. Ce tableau est très simple à construire. Il suffit de créer une colonne pour toutes les orbitales s et de placer chaque couche n sur une ligne distincte. Répétez l’opération pour les orbitales p, d et f. Veillez à n’inclure que les orbitales autorisées par les nombres quantiques (pas de 1p ou 2d, etc.). Enfin, tracez des lignes diagonales de haut en bas, comme indiqué.
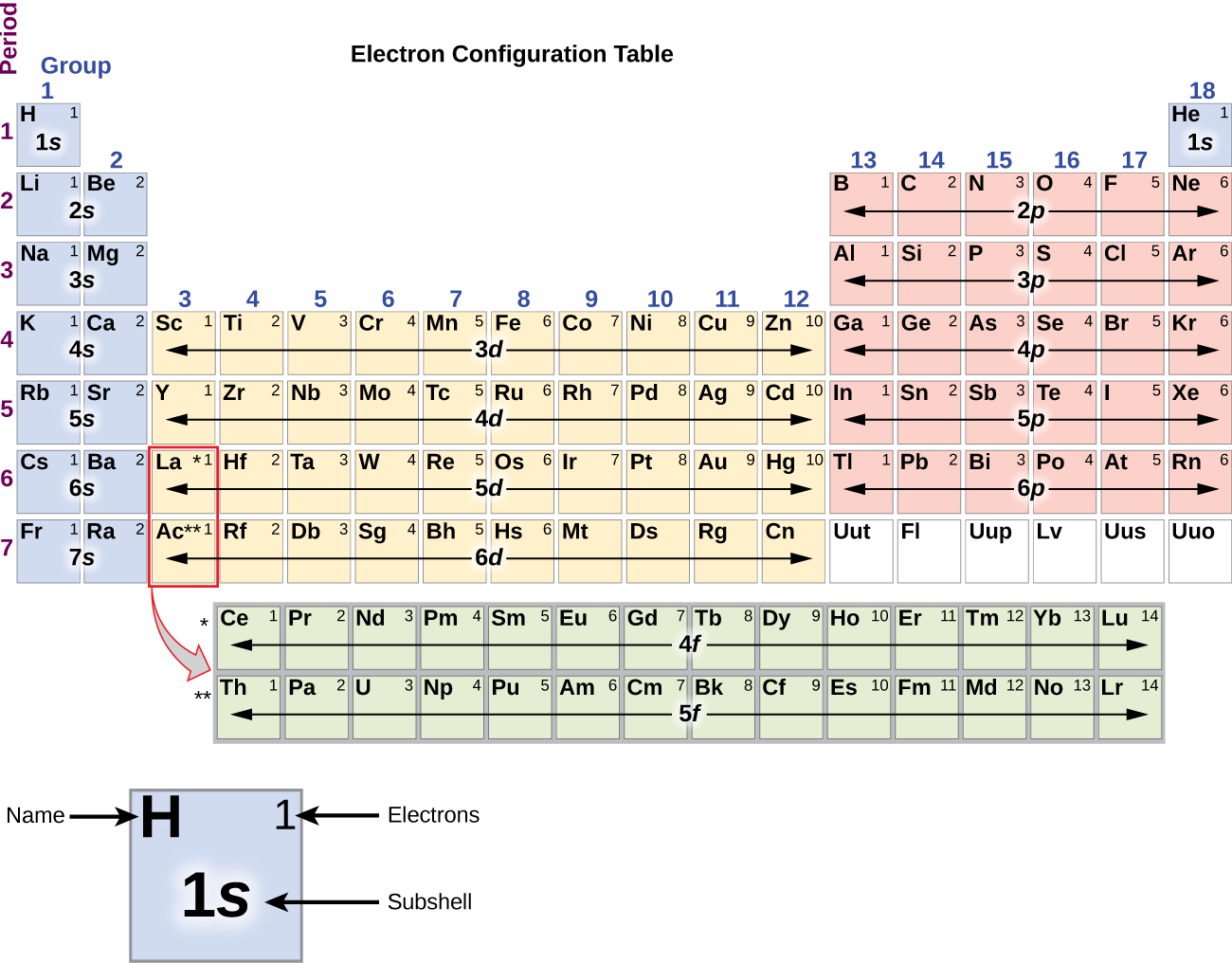
Figure 8.5.4. Ce tableau périodique indique la configuration électronique de chaque sous-couche. En « construisant » à partir de l’hydrogène, ce tableau peut être utilisé pour déterminer la configuration électronique de n’importe quel atome du tableau périodique.
Nous allons maintenant construire la configuration électronique de l’état fondamental et le diagramme orbital pour une sélection d’atomes des première et deuxième période du tableau périodique. Les diagrammes orbitaux sont des représentations picturales de la configuration électronique, montrant les orbitales individuelles et la disposition des électrons par paires. Nous commençons par un seul atome d’hydrogène (numéro atomique 1), composé d’un proton et d’un électron. En nous référant à la Figure 8.5.3. ou à la Figure 8.5.4., nous nous attendons à trouver l’électron dans l’orbitale 1s. Par convention, la valeur ms =
est généralement remplie en premier. La configuration électronique et le diagramme orbital sont:
He1 s1

1s
Après l’hydrogène se trouve l’hélium, un gaz noble dont le numéro atomique est 2. L’atome d’hélium contient deux protons et deux électrons. Le premier électron possède les quatre mêmes nombres quantiques que l’électron de l’atome d’hydrogène (n = 1, l = 0, ml = 0, ms = +12). Le deuxième électron va également dans l’orbitale 1s et remplit cette orbitale. Le deuxième électron possède les mêmes nombres quantiques n, l et ml, mais doit avoir le nombre quantique de spin opposé, soit ms = -12. Ceci est en accord avec le principe d’exclusion de Pauli: deux électrons d’un même atome ne peuvent pas avoir le même ensemble de quatre nombres quantiques. Pour les diagrammes orbitaux, cela signifie que deux flèches vont dans chaque case (représentant deux électrons dans chaque orbitale) et que les flèches doivent pointer dans des directions opposées (représentant des spins appariés). La configuration électronique et le diagramme orbital de l’hélium sont les suivants:
He1 s2

1s
La couche n = 1 est complètement remplie dans un atome d’hélium.
L’atome suivant est le lithium, un métal alcalin dont le numéro atomique est 3. Les deux premiers électrons du lithium occupent l’orbitale 1s et possèdent les mêmes ensembles de quatre nombres quantiques que les deux électrons de l’hélium. L’électron restant doit occuper l’orbitale immédiatement inférieure en énergie, l’orbitale 2s (Figure 8.5.3. ou Figure 8.5.4.). Ainsi, la configuration électronique et le diagramme orbital du lithium sont:
Li 1s2 2s1


1s 2s
Un atome de béryllium, métal alcalino-terreux de numéro atomique 4, contient quatre protons dans le noyau et quatre électrons entourant le noyau. Le quatrième électron remplit l’espace restant dans l’orbitale 2s.
Be 1s2 2s2


1s 2s
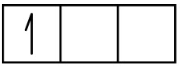
Un atome de bore (numéro atomique 5) contient cinq électrons. La couche n = 1 est remplie de deux électrons et trois électrons occuperont la couche n = 2. Comme toute sous-couche s ne peut contenir que deux électrons, le cinquième électron doit occuper le niveau d’énergie suivant, qui sera une orbitale 2p. Il existe trois orbitales 2p dégénérées (ml = -1, 0, +1) et l’électron peut occuper l’une quelconque de ces orbitales p. Lorsque nous dessinons des diagrammes d’orbitaux, nous incluons des cases vides pour représenter toute orbitale vide dans la même sous-couche que celle que nous remplissons.
B 1s2 2s2 2p1


1s 2s 2p
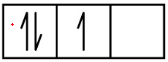
Le carbone (numéro atomique 6) possède six électrons. Quatre d’entre eux occupent les orbitales 1s et 2s. Les deux électrons restants occupent la sous-couche 2p. Nous avons maintenant le choix entre remplir l’une des orbitales 2p et apparier les électrons ou laisser les électrons non– liants dans deux orbitales p différentes, mais dégénérées. Les orbitales sont remplies comme décrit par la règle de Hund: la configuration la plus basse en énergie pour un atome avec des électrons dans un ensemble d’orbitales dégénérées est celle ayant le nombre maximum d’électrons non-liants. Ainsi, les deux électrons des orbitales 2p du carbone ont des nombres quantiques n, l et ms identiques et diffèrent par leur nombre quantique ml (conformément au principe d’exclusion de Pauli). La configuration électronique et le diagramme orbital du carbone sont les suivants:
C 1s2 2s2 2p2



1s 2s 2p
C 1s2 2s2 2p2


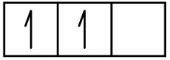

1s 2s 2p
L’azote (numéro atomique 7) remplit les sous-couches 1s et 2s et possède un électron dans chacune des trois orbitales 2p, conformément à la règle de Hund. Ces trois électrons ont des spins non-liants. L’oxygène (numéro atomique 8) possède une paire d’électrons dans l’une des orbitales 2p (les électrons ont des spins opposés) et un électron unique dans chacune des deux autres. Le fluor (numéro atomique 9) possède une seule orbitale 2p contenant un électron non-liant. Tous les électrons du gaz noble néon (numéro atomique 10) sont liés, et toutes les orbitales des couches n= 1 et n= 2 sont remplies. Les configurations électroniques et les diagrammes orbitaux de ces quatre éléments sont les suivants:
N 1s2 2s2 2p3


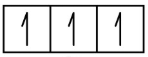
1s 2s 2p
O 1s2 2s2 2p4


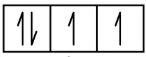
1s 2s 2p
F 1s2 2s2 2p5


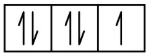
1s 2s 2p
Ne 1s2 2s2 2p6


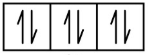
1s 2s 2p
Le sodium, métal alcalin (numéro atomique 11), possède un électron de plus que l’atome de néon. Cet électron doit aller dans la sous-couche la moins énergétique disponible, l’orbitale 3s, ce qui donne une configuration 1s22s22p63s1. Les électrons qui occupent la ou les orbitales les plus extérieures de la couche (valeur la plus élevée de n) sont appelés électrons de valence, et ceux qui occupent les orbitales intérieures de la couche sont appelés électrons de noyau (Figure 8.5.5.). Comme les orbitales de noyau correspondent aux configurations électroniques des gaz rares, nous pouvons abréger les configurations électroniques en écrivant le gaz rare qui correspond à la configuration électronique de noyau, ainsi que les électrons de valence dans un format condensé. Pour notre exemple du sodium, le symbole [Ne] représente les électrons de noyau, (1s22s22p6) et notre configuration abrégée ou condensée est [Ne]3s1.
Na 1s2 2s2 2p6 3s1
Abréviation [Ne]3 s1

Électrons de noyau Électrons de valence
Figure 8.5.5. Une configuration électronique abrégée du noyau (à droite) remplace les électrons du noyau par le symbole du gaz noble dont la configuration correspond à celle des électrons du noyau de l’autre élément.
De même, la configuration abrégée du lithium peut être représentée par [He]2s1, où [He] représente la configuration de l’atome d’hélium, qui est identique à celle de la couche interne remplie du lithium. Cette façon d’écrire les configurations met en évidence la similitude des configurations du lithium et du sodium. Ces deux atomes, qui font partie de la famille des métaux alcalins, ne possèdent qu’un seul électron dans une sous-couche de valence s dehors d’un ensemble de couches internes remplies.
Li:[He] 2s1
Na:[Ne] 3s1
Le magnésium, métal alcalino-terreux (numéro atomique 12), avec ses 12 électrons en configuration [Ne]3s2, est analogue au béryllium, [He]2s2, membre de sa famille. Les deux atomes ont une sous-couche s remplie à l’extérieur de leur couche interne remplie. L’aluminium (numéro atomique 13), avec 13 électrons et la configuration électronique [Ne]3s23p1, est analogue au bore, [He]2s22p1, membre de sa famille.
Les configurations électroniques du silicium (14 électrons), du phosphore (15 électrons), du soufre (16 électrons), du chlore (17 électrons) et de l’argon (18 électrons) sont analogues, en ce qui concerne les configurations électroniques de leurs couches externes, à celles des membres correspondants de leur famille, à savoir le carbone, l’azote, l’oxygène, le fluor et le néon, respectivement, sauf que le nombre quantique principal de la couche externe des éléments les plus lourds a augmenté d’une unité pour atteindre n = 3. La Figure 8.5.6. montre la configuration électronique la plus basse, ou état fondamental, de ces éléments ainsi que celle des atomes de chacun des éléments connus.
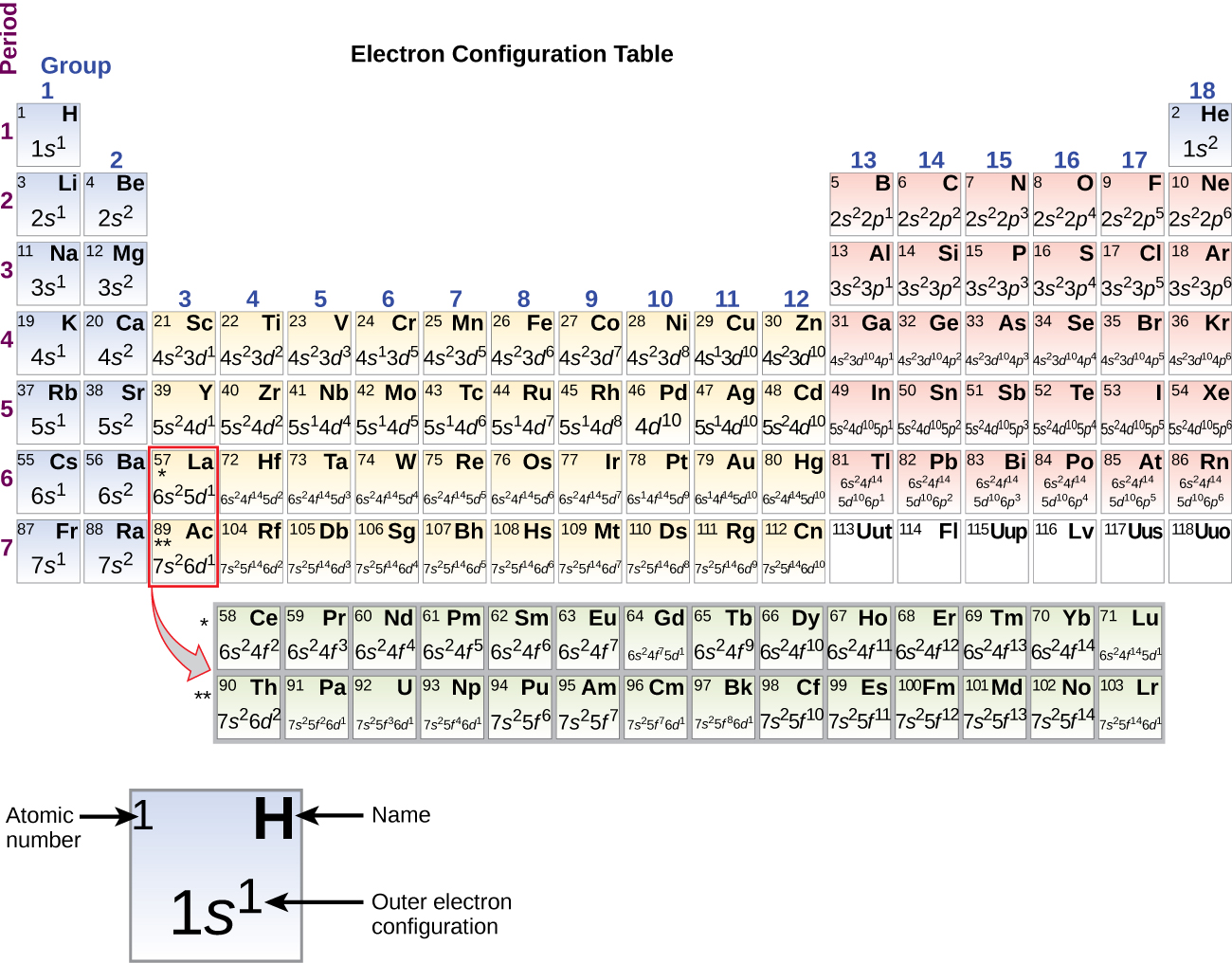
Figure 8.5.6. Cette version du tableau périodique montre la configuration électronique de la couche externe de chaque élément. Notez que dans chaque groupe, la configuration est souvent similaire.
Lorsque nous arrivons à l’élément suivant du tableau périodique, le métal alcalin potassium (numéro atomique 19), nous pourrions nous attendre à ce que nous commencions à ajouter des électrons à la sous-couche 3d. Cependant, toutes les preuves chimiques et physiques disponibles indiquent que le potassium est comme le lithium et le sodium, et que l’électron suivant n’est pas ajouté au niveau 3d mais plutôt au niveau 4s (Figure 8.5.6.). Comme nous l’avons vu précédemment, l’orbitale 3d sans nœuds radiaux a une énergie plus élevée car elle est moins pénétrante et plus protégée du noyau que la 4s, qui a trois nœuds radiaux. Ainsi, le potassium a une configuration électronique de [Ar]4s1. Par conséquent, le potassium correspond à Li et à Na dans la configuration de sa couche de valence. L’électron suivant est ajouté pour compléter la sous-couche 4s et le calcium a une configuration électronique de [Ar]4s2. Cela donne au calcium une configuration électronique de la couche externe correspondant à celle du béryllium et du magnésium.
En commençant par le métal de transition scandium (numéro atomique 21), des électrons supplémentaires sont ajoutés successivement à la sous-couche 3d. Cette sous-couche est remplie jusqu’à sa capacité de 10 électrons (rappelez-vous que pour l = 2 [orbitales d], il y a 2l + 1 = 5 valeurs de ml, ce qui signifie qu’il y a cinq orbitales d qui ont une capacité combinée de 10 électrons). La sous-couche 4p se remplit ensuite. Notez que pour trois séries d’éléments, du scandium (Sc) au cuivre (Cu), de l’yttrium (Y) à l’argent (Ag), et du lutécium (Lu) à l’or (Au), un total de 10 électrons d sont successivement ajoutés à l’orbite (n – 1) à côté de l’orbite n pour porter cette orbite (n – 1) de 8 à 18 électrons. Pour deux séries, du lanthane (La) au lutécium (Lu) et de l’actinium (Ac) au lawrencium (Lr), 14 électrons f (l = 3, 2l + 1 = 7 valeurs ml; donc sept orbitales avec une capacité combinée de 14 électrons) sont successivement ajoutés à la couche (n – 2) pour porter cette couche de 18 électrons à un total de 32 électrons.
Exemple 8.5.4 – Nombres quantiques et configurations des électrons
Quelle est la configuration électronique et le diagramme orbital d’un atome de phosphore? Quels sont les quatre nombres quantiques du dernier électron ajouté?
Solution
Le numéro atomique du phosphore est 15. Ainsi, un atome de phosphore contient 15 électrons. L’ordre de remplissage des niveaux d’énergie est 1s, 2s, 2p, 3s, 3p, 4s, …. Les 15 électrons de l’atome de phosphore se rempliront jusqu’à l’orbitale 3p, qui contiendra trois électrons:
P 1s2 2s2 2p6 3s2 3p3


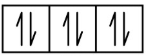

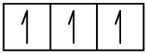
1s 2s 2p 3s 3p
Le dernier électron ajouté est un électron 3p. Par conséquent, n = 3 et, pour une orbitale de type p, l = 1. La valeur de ml pourrait être -1, 0 ou +1. Les trois orbitales p sont dégénérées, donc n’importe laquelle de ces valeurs ml est correcte. Pour les électrons non– liants, la convention attribue la valeur de +12 pour le nombre quantique de spin; ainsi, ms = +12.
Vérifiez votre apprentissage 8.5.4 – Nombres quantiques et configurations des électrons
Identifiez les atomes à partir des configurations électroniques données:
(a) [Ar]4s23d5
(b) [Kr]5s24d105p6
Réponse
(a) Mn (b) Xe
Le tableau périodique peut être un outil puissant pour prédire la configuration électronique d’un élément. Cependant, nous trouvons des exceptions à l’ordre de remplissage des orbitales qui sont illustrées dans la Figure 8.5.3. ou la Figure 8.5.4. Par exemple, les configurations électroniques (illustrées à la Figure 8.5.6.) des métaux de transition chrome (Cr; numéro atomique 24) et cuivre (Cu; numéro atomique 29), entre autres, ne sont pas celles auxquelles nous nous attendons. En général, de telles exceptions impliquent des sous-couches d’énergie très similaire, et de petits effets peuvent entraîner des changements dans l’ordre de remplissage.
Dans le cas de Cr et Cu, nous constatons que les sous-couches à moitié remplies et complètement remplies représentent apparemment des conditions de stabilité préférée.
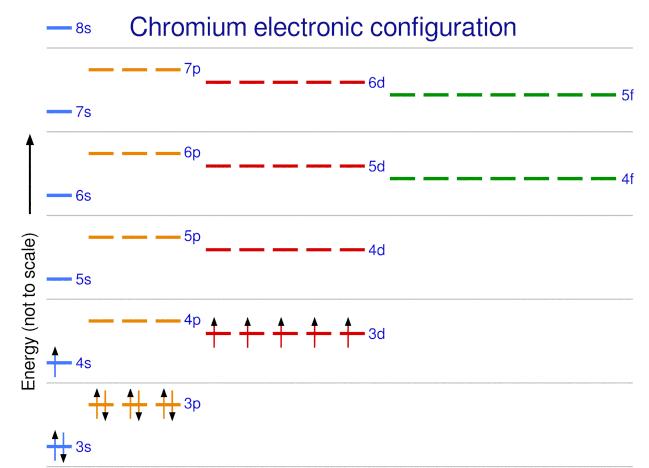
Figure 8.5.7 Configuration électronique du chrome illustrant les exceptions au remplissage de la sous-couche.
Cette stabilité est telle qu’un électron passe de l’orbitale 4s à l’orbitale 3d pour obtenir la stabilité supplémentaire d’une sous-couche 3d à moitié remplie (dans le Cr) ou d’une sous-couche 3d remplie (dans le Cu). D’autres exceptions existent également. Par exemple, le niobium (Nb, numéro atomique 41) est censé avoir la configuration électronique [Kr]5s24d3. Expérimentalement, nous observons que sa configuration électronique à l’état fondamental est en fait [Kr]5s14d4. Nous pouvons rationaliser cette observation en disant que les répulsions électron-électron subies par l’appariement des électrons dans l’orbitale 5s sont plus importantes que l’écart d’énergie entre les orbitales 5s et 4d. Il n’existe pas de méthode simple pour prédire les exceptions pour les atomes où l’ampleur des répulsions entre électrons est plus grande que les petites différences d’énergie entre les sous-couches.
Configurations des électrons et le tableau périodique
Comme nous l’avons décrit précédemment, le tableau périodique classe les atomes en fonction de leur numéro atomique croissant, de sorte que les éléments ayant les mêmes propriétés chimiques reviennent périodiquement. Lorsque leurs configurations électroniques sont ajoutées au tableau (Figure 8.5.6.), nous constatons également une récurrence périodique de configurations électroniques similaires dans les couches externes de ces éléments. Parce qu’ils se trouvent dans les couches extérieures d’un atome, les électrons de valence jouent le rôle le plus important dans les réactions chimiques. Les électrons extérieurs ont l’énergie la plus élevée des électrons d’un atome et sont plus facilement perdus ou partagés que les électrons du noyau. Les électrons de valence sont également le facteur déterminant de certaines propriétés physiques des éléments.
Les éléments d’un même groupe (ou d’une même colonne) ont le même nombre d’électrons de valence; les métaux alcalins que sont le lithium et le sodium n’ont chacun qu’un seul électron de valence, les métaux alcalino-terreux que sont le béryllium et le magnésium en ont chacun deux, et les halogènes que sont le fluor et le chlore ont chacun sept électrons de valence. La similitude des propriétés chimiques entre les éléments d’un même groupe est due au fait qu’ils ont le même nombre d’électrons de valence. C’est la perte, le gain ou le partage des électrons de valence qui définit la réaction des éléments.
Il est important de se rappeler que le tableau périodique a été élaboré sur la base du comportement chimique des éléments, bien avant que l’on ait une idée de leur structure atomique. Nous pouvons maintenant comprendre pourquoi le tableau périodique présente la disposition qu’il a – la disposition place les éléments dont les atomes ont le même nombre d’électrons de valence dans le même groupe. Cette disposition est mise en évidence dans la Figure 8.5.6, qui montre sous forme de tableau périodique la configuration électronique de la dernière sous-couche à être remplie par le principe d’Aufbau. Les sections colorées de la Figure 8.5.6. montrent les trois catégories d’éléments classées selon les orbitales remplies: éléments du groupe principal, de transition et de transition interne. Ces classifications déterminent quelles orbitales sont comptées dans la couche de valence, ou orbitales du niveau d’énergie le plus élevé d’un atome.
Les éléments du groupe principal (parfois appelés éléments représentatifs) sont ceux dans lesquels le dernier électron ajouté entre dans une orbitale s ou p dans la couche la plus externe, représentée en bleu et en rouge sur la Figure 8.5.6. Cette catégorie comprend tous les éléments non métalliques, ainsi que de nombreux métaux et les métalloïdes. Les électrons de valence des éléments du groupe principal sont ceux qui ont le niveau n le plus élevé. Par exemple, le gallium (Ga, numéro atomique 31) a la configuration électronique [Ar]4s23d104p1, qui contient trois électrons de valence (soulignés). Les orbitales d complètement remplies comptent comme des électrons de noyau et non de valence.
Éléments de transition ou métaux de transition. Ce sont des éléments métalliques dans lesquels le dernier électron ajouté entre dans une orbitale d. Les électrons de valence (ceux ajoutés après la dernière configuration de gaz noble) de ces éléments comprennent les électrons ns et (n – 1) d. La définition officielle de l’UICPA des éléments de transition spécifie ceux dont les orbitales d sont partiellement remplies. Ainsi, les éléments dont les orbitales sont complètement remplies (Zn, Cd, Hg, ainsi que Cu, Ag et Au dans la Figure 8.5.6.) ne sont pas techniquement des éléments de transition. Cependant, le terme est fréquemment utilisé pour désigner l’ensemble du bloc d (coloré en jaune dans la Figure 8.5.6.), et nous adopterons cet usage dans ce manuel.
Les éléments de transition internes sont des éléments métalliques dans lesquels le dernier électron ajouté occupe une orbitale f. Ils sont représentés en vert sur la Figure 8.5.6. Ils sont représentés en vert sur la Figure 8.5.6. Les couches de valence des éléments à transition interne sont constituées des couches (n – 2)f, (n – 1)d et ns. Il existe deux séries de transition interne:
La série des lanthanides: du lanthanide (La) au lutécium (Lu)
La série des actinides de l’actinide (Ac) au lawrencium (Lr)
Le lanthane et l’actinium, en raison de leurs similitudes avec les autres membres de la série, sont inclus et utilisés pour nommer la série, même s’il s’agit de métaux de transition sans électrons f.
Configuration des électrons des ions
Nous avons vu que les ions se forment lorsque les atomes gagnent ou perdent des électrons. Un cation (ion chargé positivement) se forme lorsqu’un ou plusieurs électrons sont retirés d’un atome parent. Les électrons de la couche ayant la plus grande valeur de n sont retirés en premier. Rappelons que le nombre quantique n indique la taille de l’orbitale (une valeur n plus élevée indique une orbitale plus grande). Ces électrons sont donc les plus éloignés du noyau et, par conséquent, les premiers à être éliminés. Cela explique pourquoi les électrons 4s sont éliminés avant les électrons 3d. Un anion (ion chargé négativement) se forme lorsqu’un ou plusieurs électrons sont ajoutés à un atome parent. Les électrons ajoutés remplissent l’ordre prédit par le principe d’Aufbau.
Exemple 8.5.5 – Prédire les configurations électroniques des ions
Quelle est la configuration électronique de:
(a) Na+
(b) P3-
(c) Al2+
(d) Fe2+
(e) Sm3+
Solution
Tout d’abord, écrivez la configuration électronique de chaque atome parent. Nous avons choisi de montrer les configurations complètes, non abrégées, afin de fournir plus de pratique aux élèves qui le souhaitent, mais la liste des configurations électroniques abrégées du noyau est également acceptable.
Ensuite, déterminez si un électron est gagné ou perdu. Rappelez-vous que les électrons sont chargés négativement, donc les ions ayant une charge positive ont perdu un électron. Pour les éléments du groupe principal, la dernière orbitale gagne ou perd un électron. Pour les métaux de transition, la dernière orbitale s perd un électron avant les orbitales d.
(a) Na: 1s22s22p63s1. Le cation sodium perd un électron, donc Na+: 1s22s22p63s1 = Na+: 1s22s22p6.
(b) P: 1s22s22p63s23p3. Le trianion phosphore gagne trois électrons, donc P3-: 1s22s22p63s23p6.
(c) Al: 1s22s22p63s23p1. Le dication d’aluminium perd deux électrons Al2+ : 1s22s22p63s23p1 =
Al2+: 1s22s22p63s1.
(d) Fe: 1s22s22p63s23p64s23d6. Le fer (II) perd deux électrons et, comme il s’agit d’un métal de transition, ils sont retirés de l’orbitale 4s Fe2+: 1s22s22p63s23p64s23d6 = 1s22s22p63s23p63d6.
(e). Sm: 1s22s22p63s23p64s23d104p65s24d105p66s24f6. La trication du samarium perd trois électrons. Les deux premiers sont perdus sur l’orbitale 6s, et le dernier est retiré de l’orbitale 4f. Sm3+: 1s22s22p63s23p64s23d104p65s24d105p66s24f6 = 1s22s22p63s23p64s23d104p65s24d105p64f5.
Vérifiez votre apprentissage 8.5.5 – Prédire les configurations électroniques des ions
Quel ion de charge +2 a la configuration électronique 1s22s22p63s23p63d104s24p64d5? Quel ion de charge +3 a cette configuration?
Réponse
Tc2+, Ru3+
★ Questions
1. En utilisant la notation complète des sous-couches (1s22s22p6, et ainsi de suite), prédisez la configuration électronique de chacun des atomes suivants:
a) N
b) Si
c) Fe
d) Te
e) Tb
2. les informations supplémentaires avons-nous besoin pour répondre à la question « Quel ion a la configuration électronique 1s22s22p63s23p6”?
3. Utilisez un diagramme orbital pour décrire la configuration électronique de la couche de valence de chacun des atomes suivants:
a) N
b) Si
c) Fe
d) Te
e) Mo
4. Quel atome a la configuration électronique 1s22s22p63s23p64s23d104p65s24d2?
5. Quel ion de charge +1 a la configuration électronique 1s22s22p63s23p63d104s24p6? Quel ion de charge -2 a cette configuration?
6. Lequel des éléments suivants possède deux électrons non-liants?
a) Mg
b) Si
c) S
d) Both Mg and S
e) Both Si and S.
7. Quel atome devrait avoir une sous-couche 4s à moitié remplie?
8. Le thallium a été utilisé comme poison dans le roman policier d’Agatha Christie « Le cheval pâle ». Le thallium a deux formes cationiques possibles, +1 et +3. Les composés +1 sont les plus stables. Écrivez la structure électronique du cation +1 du thallium.
9. Le cobalt-60 et l’iode-131 sont des isotopes radioactifs couramment utilisés en médecine nucléaire. Combien de protons, de neutrons et d’électrons y a-t-il dans les atomes de ces isotopes? Écrivez la configuration électronique complète de chaque isotope.
10. Donnez deux ensembles possibles de quatre nombres quantiques pour l’électron dans un atome H.
11. Combien de sous-couches sont complètement remplies d’électrons pour Na? Combien de sous-couches sont non remplies?
12. Quel est le nombre maximum d’électrons dans l’ensemble de la couche n = 2?
13. Écrivez la configuration électronique complète de chaque atome.
a) Si, 14 électrons
b) Sc, 21 électrons
14. Écrivez la configuration électronique complète de chaque atome.
a) Cd, 48 électrons
b) Mg, 12 électrons
15. Écrivez la configuration électronique abrégée de chaque atome de la Question 13.
16. Écrivez la configuration électronique abrégée de chaque atome de la Question 14.
17. Dessinez le diagramme d’énergie de la configuration électronique du potassium.
Réponses
1. (a) 1s2 2s2 2p3; (b) 1s2 2s2 2p6 3s2 3p2; (c) 1s2 2s2 2p6 3s2 3p6 4s2 3d6; (d) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p4; (e) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f9
2. La charge de l’ion
3.
(a)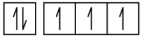
2s 2p
(b)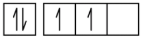
3s 3p
(c) 
4s 3d
(d)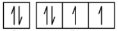
5s5p
(e)
5s4d
4. Zr
5. Rb+, Se2−
6. Bien que les points b) et c) soient tous deux corrects, le point e) englobe les deux et constitue la meilleure réponse.
7. K
8. 1s22s22p63s23p63d104s24p64d105s25p66s24f145d10
9. Le Co a 27 protons, 27 électrons et 33 neutrons: 1s22s22p63s23p64s23d7, le I a 53 protons, 53 électrons et 78 neutrons : 1s22s22p63s23p63d104s24p64d105s25p5.
10. 1, 0, 0, ½ et 1, 0, 0, -½
11. Trois sous-couches (1s, 2s, 2p) sont complètement remplies, et une couche (3s) est partiellement remplie.
12. 8 électrons
13.
a) 1s22s22p63s23p2
b) 1s22s22p63s23p64s23d1
14.
a) 1s22s22p63s23p64s23d104p65s24d10
b) 1s22s22p63s2
15. [Ne]3s23p2
16. [Ar]4s23d1
17.
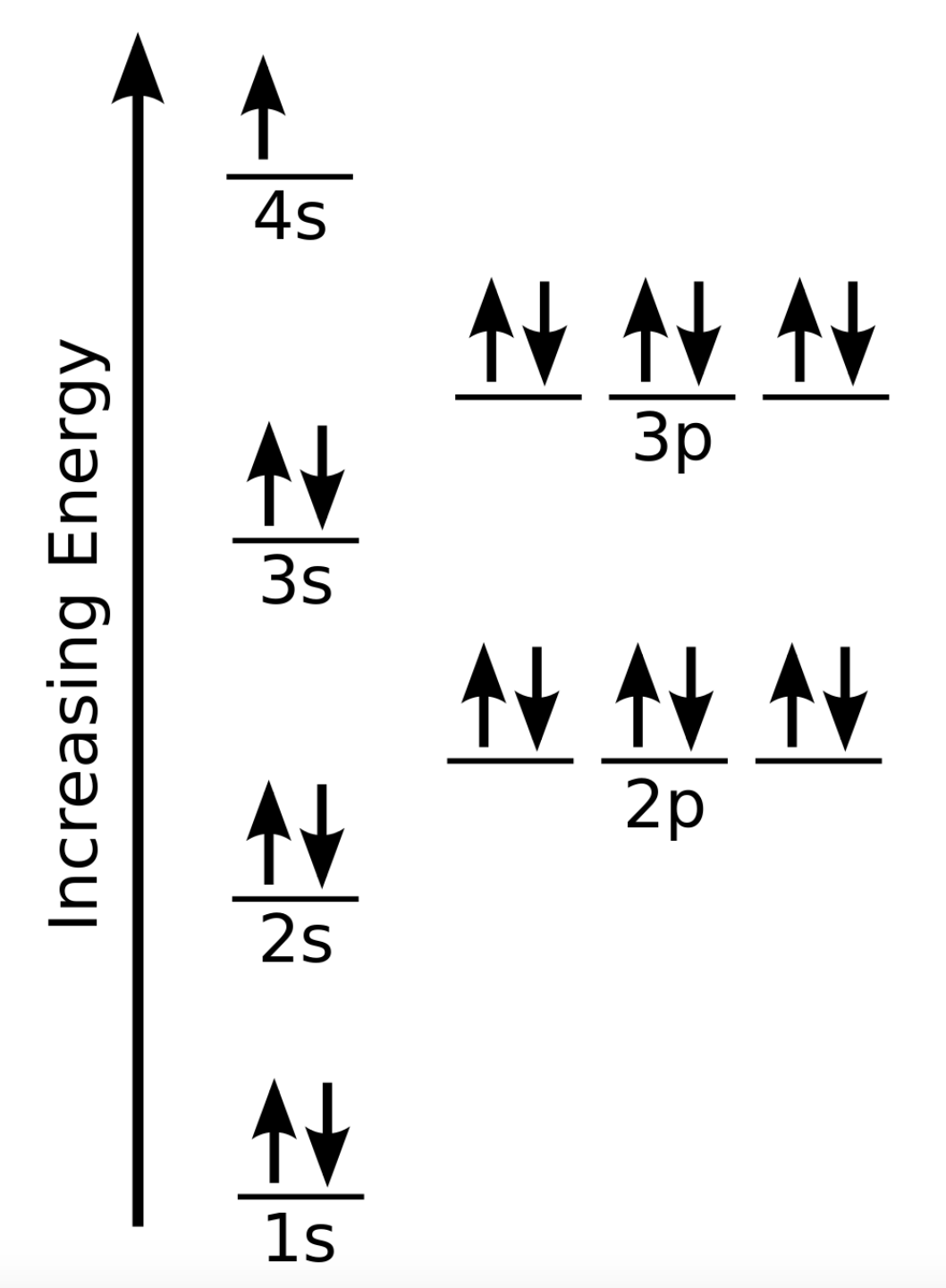
Spécifie qu'aucun électron dans un atome ne peut avoir la même valeur pour les quatre nombres quantiques
Liste qui identifie l'occupation en électrons des coquilles et sous-coquilles d'un atome
Procédure dans laquelle la configuration électronique des éléments est déterminée en les "construisant" dans l'ordre des numéros atomiques, en ajoutant un proton au noyau et un électron à la sous-coque appropriée à la fois ; les électrons remplissent d'abord les orbiteales de plus faible énergie
Représentation picturale de la configuration des électrons montrant chaque orbite sous forme de boîte et chaque électron sous forme de flèche
Chaque orbite d'une sous-coque est occupée par un seul électron avant qu'une autre orbite ne soit doublement occupée, et tous les électrons des orbites occupées par un seul électron ont le même spin
Électrons de la coque extérieure ou de valence (valeur la plus élevée de n) plus les électrons de la dernière sous-coque non remplie d'un atome de terre ; les électrons les plus probablement impliqués dans les réactions chimiques
Électron dans un atome qui occupe les orbites des coquilles intérieures
Coquille d'électrons la plus haute et la plus externe d'un atome de terre

