6.4 ATP : Adénosine Triphosphate
Objectifs d’apprentissage
À la fin de cette section, vous serez en mesure de faire ce qui suit :
- Expliquer le rôle de l’ATP en tant que monnaie d’échange de l’énergie cellulaire
- Décrire comment l’énergie est libérée par l’hydrolyse de l’ATP
Même les réactions exergoniques, qui libèrent de l’énergie, nécessitent une petite quantité d’énergie d’activation pour se produire. En revanche, les réactions endergoniques nécessitent un apport d’énergie beaucoup plus important, car leurs produits ont plus d’énergie libre que leurs réactifs. Au sein de la cellule, d’où provient l’énergie nécessaire à ces réactions ? La réponse se trouve dans une molécule de fourniture d’énergie que les scientifiques appellent l’adénosine triphosphate, ou ATP. Il s’agit d’une petite molécule relativement simple (Figure 6.13), mais qui contient, dans certaines de ses liaisons, le potentiel d’une poussée rapide d’énergie qui peut être exploitée pour effectuer un travail cellulaire. Considérez cette molécule comme la principale monnaie énergétique des cellules, de la même manière que l’argent est la monnaie que les gens échangent pour obtenir les choses dont ils ont besoin. L’ATP alimente la majorité des réactions cellulaires nécessitant de l’énergie.

Comme son nom l’indique, l’adénosine triphosphate est composée d’adénosine liée à trois groupes phosphates (Figure 6.13). L’adénosine est un nucléoside composé de la base azotée adénine et d’un sucre à cinq carbones, le ribose. Les trois groupes phosphates, dans l’ordre du plus proche au plus éloigné du sucre ribose, sont l’alpha, le bêta et le gamma. Ensemble, ces groupes chimiques constituent une centrale énergétique. Cependant, toutes les liaisons de cette molécule n’existent pas dans un état d’énergie particulièrement élevé. Les deux liaisons qui relient les phosphates sont également des liaisons à haute énergie (liaisons phosphoanhydrides) qui, lorsqu’elles sont rompues, libèrent suffisamment d’énergie pour alimenter toute une série de réactions et de processus cellulaires. Ces liaisons à haute énergie sont les liaisons entre les deuxième et troisième (ou bêta et gamma) groupes phosphates et entre les premier et deuxième groupes phosphates. Ces liaisons sont à « haute énergie » parce que les produits de cette rupture de liaison – l’adénosine diphosphate (ADP) et un groupe phosphate inorganique (Pi) – ont une énergie libre considérablement inférieure à celle des réactifs : ATP et molécule d’eau. Comme cette réaction se produit en utilisant une molécule d’eau, il s’agit d’une réaction d’hydrolyse. En d’autres termes, l’ATP s’hydrolyse en ADP dans la réaction suivante :
ATP + H2O → ADP + Pi + énergie libre
Comme la plupart des réactions chimiques, l’hydrolyse de l’ATP en ADP est réversible. La réaction inverse régénère l’ATP à partir de l’ADP +Pi. Les cellules dépendent de la régénération de l’ATP tout comme les gens dépendent de la régénération de l’argent dépensé par le revenu. Comme l’hydrolyse de l’ATP libère de l’énergie, la régénération de l’ATP doit nécessiter un apport d’énergie libre. Cette équation exprime la formation d’ATP :
ADP + Pi + énergie libre → ATP + H2O
Deux questions importantes restent en suspens en ce qui concerne l’utilisation de l’ATP comme source d’énergie. Quelle est la quantité exacte d’énergie libre libérée lors de l’hydrolyse de l’ATP et comment cette énergie libre effectue-t-elle le travail cellulaire ? Le ∆G calculé pour l’hydrolyse d’une mole d’ATP en ADP et Pi est de -7,3 kcal/mole (-30,5 kJ/mol). Puisque ce calcul est vrai dans des conditions standard, on peut s’attendre à ce qu’une valeur différente existe dans des conditions cellulaires. En fait, le ∆G pour l’hydrolyse d’une mole d’ATP dans une cellule vivante est presque le double de la valeur dans des conditions normales : -14 kcal/mol (-57 kJ/mol).
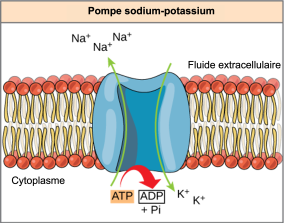
L’ATP est une molécule très instable. S’il n’est pas utilisé rapidement pour effectuer un travail, l’ATP se dissocie spontanément en ADP + Pi, et l’énergie libre libérée au cours de ce processus est perdue sous forme de chaleur. La deuxième question que nous avons posée ci-dessus porte sur la manière dont la libération d’énergie par hydrolyse de l’ATP effectue un travail à l’intérieur de la cellule. Cela dépend d’une stratégie que les scientifiques appellent le couplage énergétique. Les cellules couplent la réaction exergonique de l’hydrolyse de l’ATP, ce qui leur permet de se poursuivre. Un exemple de couplage énergétique utilisant l’ATP implique une pompe ionique transmembranaire extrêmement importante pour la fonction cellulaire. Cette pompe sodium-potassium (pompe Na+/K+) fait sortir le sodium de la cellule et fait entrer le potassium dans la cellule (Figure 6.14). Un pourcentage important de l’ATP d’une cellule alimente cette pompe, car les processus cellulaires font entrer une quantité considérable de sodium dans la cellule et en font sortir du potassium. La pompe travaille constamment pour stabiliser les concentrations cellulaires de sodium et de potassium. Pour que la pompe effectue un cycle (exportation de trois ions Na+ et importation de deux ions K+), une molécule d’ATP doit s’hydrolyser. Lorsque l’ATP s’hydrolyse, son phosphate gamma ne s’envole pas simplement, mais se transfère sur la protéine de la pompe. Les scientifiques appellent ce processus de liaison d’un groupe phosphate à une molécule la phosphorylation. Comme dans la plupart des cas d’hydrolyse de l’ATP, un phosphate de l’ATP est transféré sur une autre molécule. Dans un état phosphorylé, la pompe Na+/K+ a plus d’énergie libre et est amenée à subir un changement de conformation. Ce changement lui permet de libérer du Na+ à l’extérieur de la cellule. Elle lie ensuite le K+ extracellulaire, ce qui, par un autre changement de conformation, entraîne le détachement du phosphate de la pompe. Cette libération de phosphate déclenche la libération de K+ à l’intérieur de la cellule. Essentiellement, l’énergie libérée par l’hydrolyse de l’ATP est couplée à l’énergie nécessaire pour alimenter la pompe et transporter les ions Na+ et K+. L’ATP effectue le travail cellulaire en utilisant cette forme de base de couplage énergétique par phosphorylation.
Lien visuel
Souvent, au cours des réactions métaboliques cellulaires, telles que la synthèse et la dégradation des nutriments, certaines molécules doivent modifier légèrement leur conformation pour devenir des substrats pour l’étape suivante de la série de réactions. Par exemple, lors des toutes premières étapes de la respiration cellulaire, lorsqu’une molécule de glucose se décompose au cours du processus de glycolyse. Dans la première étape, l’ATP est nécessaire pour phosphoryler le glucose, créant ainsi un intermédiaire instable, mais à haute teneur énergétique. Cette réaction de phosphorylation entraîne un changement de conformation qui permet à la molécule de glucose phosphorylée de se transformer en fructose, un sucre phosphorylé. Le fructose est un intermédiaire nécessaire à la progression de la glycolyse. Ici, la réaction exergonique de l’hydrolyse de l’ATP s’associe à la réaction endergonique de conversion du glucose en un intermédiaire phosphorylé dans la voie. Une fois de plus, l’énergie libérée par la rupture d’une liaison phosphate au sein de l’ATP a été utilisée pour phosphoryler une autre molécule, créant ainsi un intermédiaire instable et entraînant un important changement de conformation.

