5.3 Transport actif
Objectifs d’apprentissage
À la fin de cette section, vous serez en mesure de faire ce qui suit :
- Comprendre comment les gradients électrochimiques affectent les ions
- Distinguer entre le transport actif primaire et le transport actif secondaire
Les mécanismes de transport actif nécessitent l’énergie de la cellule, habituellement sous forme d’adénosine triphosphate (ATP). Si une substance doit pénétrer dans la cellule en fonction de son gradient de concentration, c’est-à-dire si la concentration de la substance à l’intérieur de la cellule est supérieure à sa concentration dans le fluide extracellulaire (et vice versa), la cellule doit utiliser de l’énergie pour déplacer la substance. Certains mécanismes de transport actifs déplacent les matériaux de faible poids moléculaire, comme les ions, à travers la membrane. D’autres mécanismes transportent des molécules beaucoup plus grosses.
Gradient électrochimique
Nous avons discuté des gradients de concentration simples — les concentrations différentielles d’une substance dans un espace ou une membrane — mais dans les systèmes vivants, les gradients sont plus complexes. Comme les ions entrent et sortent des cellules et parce que les cellules contiennent des protéines qui ne se déplacent pas à travers la membrane et qui sont principalement chargées négativement, il y a aussi un gradient électrique, une différence de charge, à travers la membrane plasmique. L’intérieur des cellules vivantes est électriquement négatif par rapport au liquide extracellulaire dans lequel elles sont baignées, et en même temps, les cellules ont des concentrations plus élevées de potassium (K+) et des concentrations de sodium (Na+) plus faibles que le liquide extracellulaire. Ainsi, dans une cellule vivante, le gradient de concentration de Na+ a tendance à l’entraîner dans la cellule, et son gradient électrique (un ion positif) l’entraîne également vers l’intérieur chargé négativement. Cependant, la situation est plus complexe pour d’autres éléments comme le potassium. Le gradient électrique du K+, un ion positif, le fait entrer dans la cellule, mais le gradient de concentration du K+ fait sortir le K+ de la cellule (Figure 5.16) [lien vers Biology 2e]. Nous appelons le gradient de concentration combiné et la charge électrique qui affecte un ion son gradient électrochimique.
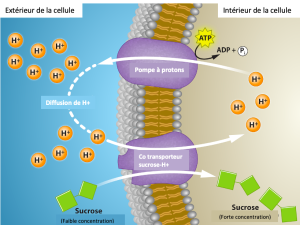
Déplacement à l’encontre d’un gradient
Pour déplacer les substances contre une concentration ou un gradient électrochimique, la cellule doit utiliser de l’énergie. Cette énergie provient de l’ATP généré par le métabolisme de la cellule. Les mécanismes de transport actifs, ou pompes, agissent contre les gradients électrochimiques. Les petites substances passent constamment à travers les membranes plasmiques. Le transport actif maintient les concentrations d’ions et d’autres substances dont les cellules vivantes ont besoin face à ces mouvements passifs. Une cellule peut dépenser une grande partie de son apport en énergie métabolique pour maintenir ces processus. (Un globule rouge utilise la majeure partie de son énergie métabolique pour maintenir le déséquilibre entre les niveaux extérieurs et intérieurs de sodium et de potassium dont la cellule a besoin.) Comme les mécanismes de transport actif dépendent du métabolisme d’une cellule pour l’énergie, ils sont sensibles à de nombreux poisons métaboliques qui interfèrent avec l’apport d’ATP.
Il existe deux mécanismes de transport de matériaux de faible poids moléculaire et de petites molécules. Le transport actif primaire déplace les ions à travers une membrane et crée une différence de charge à travers cette membrane, qui dépend directement de l’ATP. Le transport actif secondaire ne nécessite pas directement l’ATP : il s’agit plutôt du mouvement du matériau dû au gradient électrochimique établi par le transport actif primaire.
Transporteurs pour le transport actif
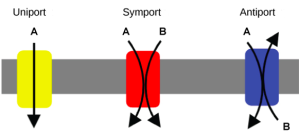
Une adaptation membranaire importante pour le transport actif est la présence de protéines porteuses spécifiques ou de pompes pour faciliter le mouvement : il existe trois types de protéines ou porteurs (Figure 5.18). Un uniport porte un ion ou une molécule spécifique. Un symport transporte deux ions ou molécules différents, tous deux dans la même direction. Un antiport transporte également deux ions ou molécules différents, mais dans des directions différentes. Tous ces transporteurs peuvent également transporter de petites molécules organiques non chargées, comme le glucose. Ces trois types de protéines porteuses sont également en diffusion facilitée, mais ils n’ont pas besoin de l’ATP pour fonctionner dans ce processus. Quelques exemples de pompes pour le transport actif sont la Na+-K+ATPase, qui transporte les ions sodium et potassium, et la H+-K+ATPase, qui transporte des ions hydrogène et potassium. Ces deux protéines sont porteuses d’antiports. Deux autres protéines porteuses sont la Ca2+ ATPase et la H+ ATPase, qui ne transportent que des ions calcium et des ions hydrogène, respectivement. Les deux sont des pompes.
Transport actif primaire
Le transport actif primaire qui fonctionne avec le transport actif du sodium et du potassium permet le transport actif secondaire. La deuxième méthode de transport est toujours active parce qu’elle dépend de l’utilisation de l’énergie comme le transport primaire (Figure 5.19).

L’une des pompes les plus importantes dans les cellules animales est la pompe sodium-potassium (Na+-K+ATPase), qui maintient le gradient électrochimique (et les concentrations correctes de Na+ et K+) dans les cellules vivantes. La pompe sodium-potassium déplace K+ dans la cellule tout en déplaçant Na+ en même temps, à un rapport de trois Na+ pour chaque deux ions K+ déplacés. La Na+-K+ATPase existe sous deux formes, selon son orientation vers l’intérieur ou l’extérieur de la cellule et son affinité pour les ions sodium ou potassium. Le processus comporte les six étapes suivantes.
- L’enzyme étant orientée vers l’intérieur de la cellule, le transporteur a une affinité élevée pour les ions sodium. Trois ions se lient à la protéine.
- Le transporteur protéique hydrolyse l’ATP et un groupe phosphate de faible énergie s’y rattache.
- Par conséquent, le support change de forme et se réoriente vers l’extérieur de la membrane. L’affinité de la protéine pour le sodium diminue et les trois ions sodium quittent le support.
- Le changement de forme augmente l’affinité du porteur pour les ions potassium, et deux de ces ions se fixent à la protéine. Par la suite, le groupe phosphate de faible énergie se détache du support.
- Lorsque le groupe phosphate est éliminé et que les ions potassium sont attachés, la protéine porteuse se repositionne vers l’intérieur de la cellule.
- La protéine porteuse, dans sa nouvelle configuration, a une affinité réduite pour le potassium, et les deux ions se déplacent dans le cytoplasme. La protéine a maintenant une affinité plus élevée pour les ions sodium, et le processus recommence.
Plusieurs choses se sont produites à la suite de ce processus. À ce stade, il y a plus d’ions sodium à l’extérieur de la cellule qu’à l’intérieur et plus d’ions potassium à l’intérieur qu’à l’extérieur. Pour tous les trois ions sodium qui sortent, deux ions potassium entrent. Il en résulte que l’intérieur est légèrement plus négatif par rapport à l’extérieur. Cette différence de charge est importante pour créer les conditions nécessaires au processus secondaire. La pompe sodium-potassium est donc une pompe électrogène (une pompe qui crée un déséquilibre de charge), créant un déséquilibre électrique à travers la membrane et contribuant au potentiel de la membrane.
Transport actif secondaire (co-transport)
Le transport actif secondaire utilise l’énergie cinétique des ions sodium pour amener d’autres composés, contre leur gradient de concentration dans la cellule. À mesure que les concentrations d’ions sodium s’accumulent à l’extérieur de la membrane plasmique en raison du processus de transport actif primaire, cela crée un gradient électrochimique. Si une protéine de canal existe et est ouverte, les ions sodium diminueront de son gradient de concentration à travers la membrane. Ce mouvement transporte d’autres substances qui doivent être attachées à la même protéine de transport pour que les ions sodium se déplacent à travers la membrane (Figure 5.20 [lien vers Biology 2e]). De nombreux acides aminés, ainsi que le glucose, pénètrent dans une cellule de cette façon. Ce procédé secondaire stocke également des ions hydrogène à haute énergie dans les mitochondries de cellules végétales et animales afin de produire de l’ATP. L’énergie potentielle qui s’accumule dans les ions hydrogène emmagasinés se traduit par une énergie cinétique lorsque les ions traversent la protéine ATP synthase, et cette énergie convertit ensuite l’ADP en ATP.

