16.3 Régulation épigénétique des gènes chez les eucaryotes
Objectifs d’apprentissage
À la fin de cette section, vous serez en mesure de faire ce qui suit :
- Expliquer comment le remodelage de la chromatine contrôle l’accès à la transcription
- Décrire comment l’accès à l’ADN est contrôlé par la modification des histones
- Décrire le lien entre la méthylation de l’ADN et les modifications épigénétiques des gènes
L’expression des gènes eucaryotes est plus complexe que celle des gènes procaryotes, car les processus de transcription et de traduction sont physiquement séparés. Contrairement aux cellules procaryotes, les cellules eucaryotes peuvent réguler l’expression génique à différents niveaux. Les modifications épigénétiques sont des modifications héréditaires de l’expression génique qui ne résultent pas de changements dans la séquence de l’ADN. L’expression des gènes eucaryotes commence par le contrôle de l’accès à l’ADN. L’accès de la transcription à l’ADN peut être contrôlé de deux manières générales : le remodelage de la chromatine et la méthylation de l’ADN. Le remodelage de la chromatine modifie la façon dont l’ADN est associé aux histones chromosomiques. La méthylation de l’ADN est associée à des changements dans le développement et au silençage génique.
Contrôle épigénétique : Régulation de l’accès aux gènes dans le chromosome
Le génome humain code pour plus de 20 000 gènes, avec des centaines voire des milliers de gènes sur chacun des 23 chromosomes humains. L’ADN dans le noyau est précisément enroulé, plié et compacté en chromosomes pour qu’il s’insère dans le noyau. Il est également organisé de manière à ce que des segments spécifiques puissent être accessibles en fonction des besoins d’un type de cellule spécifique.
Le premier niveau d’organisation, ou d’empaquetage, est l’enroulement des brins d’ADN autour des protéines histones. Les histones regroupent et ordonnent l’ADN en unités structurelles appelées complexes nucléosomiques, qui peuvent contrôler l’accès des protéines aux régions de l’ADN (figure 16.7a). Au microscope électronique, cet enroulement de l’ADN autour des protéines histones pour former des nucléosomes ressemble à de petites perles sur un fil (figure 16.7b).
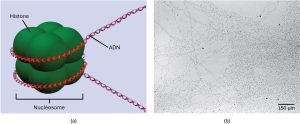
Ces perles (protéines d’histone) peuvent se déplacer le long de la corde (ADN) pour exposer différentes sections de la molécule. Si l’ADN codant pour un gène spécifique doit être transcrit en ARN, les nucléosomes entourant cette région de l’ADN peuvent glisser le long de l’ADN pour ouvrir cette région chromosomique spécifique et permettre à la machinerie transcriptionnelle (ARN polymérase) d’initier la transcription (figure 16.8).
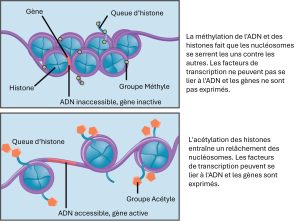
Le degré d’association des protéines histones avec l’ADN est régulé par des signaux présents à la fois sur les protéines histones et sur l’ADN. Ces signaux sont des groupes fonctionnels ajoutés aux protéines histones ou à l’ADN et déterminent si une région chromosomique doit être ouverte ou fermée (La figure 16.9 illustre les modifications apportées aux protéines histones et à l’ADN). Ces étiquettes ne sont pas permanentes, mais peuvent être ajoutées ou supprimées selon les besoins. Certains groupements chimiques (groupements phosphate, méthyle ou acétyle) sont attachés à des acides aminés spécifiques dans les « queues » d’histones à l’extrémité N-terminale de la protéine. Ces groupes ne modifient pas la séquence des bases de l’ADN, mais ils modifient le degré d’enroulement de l’ADN autour des protéines histones. L’ADN est une molécule chargée négativement et les histones non modifiées sont chargées positivement ; par conséquent, les changements de charge de l’histone modifieront le degré d’enroulement de la molécule d’ADN. En ajoutant des modifications chimiques telles que des groupes acétyles, la charge devient moins positive et la liaison de l’ADN aux histones est relâchée. La modification de l’emplacement des nucléosomes et de l’étanchéité de la liaison des histones ouvre certaines régions de la chromatine à la transcription et en ferme d’autres.
La molécule d’ADN elle-même peut également être modifiée par méthylation. La méthylation de l’ADN se produit dans des régions très spécifiques appelées îlots CpG. Il s’agit de tronçons présentant une fréquence élevée de paires d’ADN de dinucléotides cytosine et guanosine (CG), que l’on trouve dans les régions promotrices des gènes. La cytosine de la paire CG peut être méthylée (ajout d’un groupe méthyle). Les gènes méthylés sont généralement réduits au silence, bien que la méthylation puisse avoir d’autres effets régulateurs. Dans certains cas, les gènes qui sont réduits au silence pendant le développement des gamètes d’un parent sont transmis dans leur état silencieux à la progéniture. Ces gènes sont dits imprégnés. Le régime alimentaire des parents ou d’autres conditions environnementales peuvent également affecter les schémas de méthylation des gènes, ce qui modifie l’expression génique. Les modifications de l’organisation de la chromatine interagissent avec la méthylation de l’ADN. Les ADN méthyltransférases semblent être attirés par les régions de la chromatine présentant des modifications spécifiques des histones. Les régions d’ADN fortement méthylées (hyperméthylées) avec des histones désacétylées sont étroitement condensées et transcriptionnellement inactives.
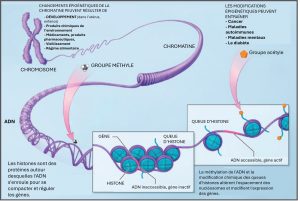
Les modifications épigénétiques ne sont pas permanentes, bien qu’elles persistent souvent à travers plusieurs cycles de division cellulaire et peuvent même traverser les générations. Le remodelage de la chromatine modifie la structure chromosomique (ouverte ou fermée) en fonction des besoins. Si un gène doit être transcrit, les protéines histones et l’ADN de la région chromosomique codant pour ce gène sont modifiés de manière à ouvrir la région promotrice pour permettre à l’ARN polymérase et à d’autres protéines, appelées facteurs de transcription, de se lier et d’initier la transcription. Si un gène doit rester désactivé, ou réduit au silence, les protéines histones et l’ADN subissent différentes modifications qui signalent une configuration chromosomique fermée. Dans cette configuration fermée, l’ARN polymérase et les facteurs de transcription n’ont pas accès à l’ADN et la transcription ne peut avoir lieu (figure 16.9).

