3 Chapitre 3 – Les analyses des gaz du sang
Partie A : Les compensations normales physiologiques en présence de déséquilibres acido-basique
Partie B : Quelques petits trucs pour compléter l’analyse des gaz du sang
Partie A
Les déséquilibres acido-basique qui affectent le pH sanguin sont reliés aux changements du gaz carbonique sanguin, la PCO2, et aux changements du bicarbonate (HCO3). Lorsqu’on fait un prélèvement sanguin on injecte le sang dans une machine qui fait l’analyse. Des électrodes mesurent directement le pH et la PCO2. L’électrode Sanz mesure le pH sanguin et l’électrode Severinghaus mesure la PCO2. Le HCO3– est mesuré indirectement. La machine d’analyse calcule le niveau de HCO3 en utilisant l’équation mathématique Henderson-Hasselbach.
En plus d’analyser les changements de pH, PCO2 et HCO3 sanguin on analyse aussi l’oxygénation du sang. L’électrode Clark mesure directement la PO2 dissoute dans le sang. La SO2 est ensuite calculer par la machine par l’intermédiaire de la courbe de dissociation de l’oxygène. Les mesures directes de la saturation (SpO2), du monoxyde de carbone (HbCO) et de la méthémoglobien (MetHb) se font via la spectrophotométrie (l’oxymétrie fractionnelle).
Les niveaux de pH, PCO2, HCO3, PO2, SO2 peuvent être tous mesurés dans le sang artériel ou veineux. On va vouloir analyser les composantes artérielles pour analyser le fonctionnement pulmonaire. Si on veut seulement estimer l’oxygénation sanguine on peut analyser les valeurs veineuses.
Le gaz carbonique artériel, la PaCO2, normale se situe entre 35 – 45 mmHg. Cette valeur est influencé par le métabolisme cellulaire et la ventilation alvéolaire. La PvCO2 est environ 3 – 8 mmHg en-dessous des valeurs artérielles.
Le HCO3 artériel normal se situe entre 22 – 26 mEq/L. Le HCO3 veineux est environ 1 – 2 mEq/L plus élevé que la valeur artérielle. Cette valeur est influencé par la filtration, la réabsorption et l’excrétion rénale et aussi varie selon le niveau de la PCO2. Le niveau de la PCO2 influence la valeur du HCO3 suite aux variations créer par la réaction d’hydrolyse.
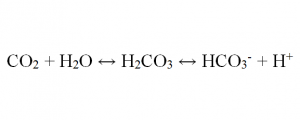
Si le niveau de PCO2 augmente l’équation est déviée vers la droite augmentant ainsi l’acide carbonique et le bicarbonate sanguin.
Si le niveau de PCO2 diminue l’équation est déviée vers la gauche diminuant ainsi l’acide carbonique et le bicarbonate sanguin.
Pour classifier et interpréter les changements physiologiques acido-basique on doit comprendre comment les poumons et les reins compensent lorsqu’il existe un déséquilibre. Si le déséquilibre cause un changement du HCO3 l’organe qui essayera de compenser pour rétablir un pH normal sera le poumon. Si le déséquilibre cause un changement de la PCO2 l’organe qui essayera de compenser pour rétablir un pH normal sera le rein.
Par exemple, si un patient souffre d’un problème rénal diminuant le niveau de HCO3 et le pH, la ventilation alvéolaire devrait augmenter immédiatement. Cette hyperventilation diminue la PaCO2 et rehausse le pH. Si le patient souffre d’une hypoventilation les reins devraient réabsorber du HCO3 augmentant davantage le pH. À noter que les reins répondent plus lentement que les poumons. La compensation rénale nécessite 24 – 72 heures.
Les compensations normales physiologiques en présence de déséquilibres acido-basique
ACIDOSE RESPIRATOIRE
L’acidose respiratoire est définie comme étant une PaCO2 qui augmente au-dessus de la limite normale de 45 mmHg.
Les causes sont associées à une diminution de la ventilation alvéolaire qui diminue l’excrétion de la PaCO2 ou à une augmentation du métabolisme cellulaire qui n’est pas accompagné par une augmentation de la ventilation alvéolaire.
Les causes d’une diminution de la ventilation alvéolaire :
- un désordre neurologique qui affecte les centres respiratoires
- un désordre nerveux qui affecte la transmission nerveuse vers les muscles squelettiques
- un désordre au niveau de la jonction neuromusculaire
- un désordre musculaire
- une fatigue musculaire
Les causes qui augmentent le métabolisme cellulaire :
- une fièvre
- un traumatisme tissulaire
- le grand brûlé
- l’hyperthyroïdie
En présence d’une augmentation de la PaCO2 l’organe qui ramène l’équilibre physiologique est le rein. La compensation se fait via une réabsorption du tampon bicarbonate (HCO3) et une excrétion des protons. Cette compensation nécessite 24 – 72 heures. La compensation peut être complète surtout si la PaCO2 n’augmente pas plus que 60 – 65 mmHg.
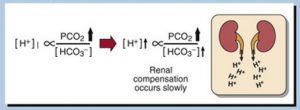
⬆ PaCO2 70 mmHg ⇒ pH 7.22, HCO3 27
Compensation rénale ⇒ pH 7.31, HCO3 31
Remarquer qu’avec l’exemple ci-dessus le pH n’est pas revenu à une valeur normale de 7.35 car la PaCO2 a augmenté au-delà de la compensation physiologique possible (PaCO2 > 60 – 65 mmHg)
En plus d’entraîner des changements acido basique, un changement de la PaCO2 va automatiquement causer une variation au niveau du bicarbonate provoquer par la réaction d’hydrolyse.
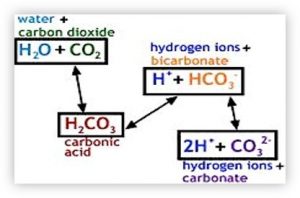
Exemple :
La PaCO2 passe de 40 mmHg à PaCO2 70 mmHg
-
-
-
- pour l’hypercapnée le HCO3 augmente de 1 meq/L avec chaque augmentation de la PaCO2 de 10 mmHg
- avec l’exemple ci-dessus le HCO3 va augmenter de 3 mEq/L
- le nouveau pH sans compensation rénale serait de 7.22 (3 X 0.06 = 0.18 : 7.40 – 0.18 = 7.22) et le HCO3 serait de 27 – 29 mEq/L
- avec une compensation rénale le nouveau pH serait environ 7.31 – 7.33 et le HCO3 serait de 30 – 33 mEq/L; le changement dans le niveau du bicarbonate comprend les changements provoquer par la réaction d’hydrolyse et la réabsorption rénale suite à la compensation
-
-
ALCALOSE RESPIRATOIRE
Une alcalose respiratoire est définie comme étant une diminution de la PaCO2 en-dessous de la limite normale de 35 mmHg.
Les causes sont associées à une augmentation de la ventilation alvéolaire qui augmente l’excrétion de la PaCO2 ou à une diminution du métabolisme cellulaire qui n’est pas accompagné par une diminution de la ventilation alvéolaire.
Les causes d’une augmentation de la ventilation alvéolaire :
- anxitété
- stimulatin des centres respiratoires (accident cérébrovasculaire ischémique, infection, toxicité d’acide salycilate)
- hypoxie
- hypoxémie surtout quand la PaO2 < 65 mmHg (stimulation des chémorécepteurs périphériques)
- stimulation des récepteurs irritants, récepteurs J ex : intubation avec tube endotrachéal, désordre pulmonaire affectant la membrane alvéolo-capillaire, embolie pulmonaire, troisième trimestre
Les causes qui diminuent le métabolisme cellulaire :
- l’hypothermie
- l’hypothyroïdie
En présence d’une diminution de la PaCO2 l’organe qui ramène l’équilibre physiologique est le rein. La compensation se fait via une diminution de la réabsorption du tampon bicarbonate – HCO3. Cette compensation nécessite 24 – 72 heures. Cette compensation généralement retourne la pH à mi-chemin à moins que cette compensation se poursuit pendant plusieurs semaines. Si la compensation est complète les reins ne provoqueront pas une diminution du HCO3 en-dessous de 15 mEq/L.
La réaction d’hydrolyse s’effectue aussi quand la PaCO2 diminue. Pour l’hypocapnée le HCO3 diminue de 1 mEq/L pour chaque diminution de 5 mEq/L.
Exemple :
La PaCO2 passe de 40 mmHg à 20 mmHg
-
-
- le HCO3 va diminuer de 4 mEq/L suite à la réaction d’hydrolye
- le nouveau pH sans compensation serait un pH de 7.60 avec un HCO3 de 18 – 20 mEq/L
- s’il y a compensation rénale le nouveau pH serait de 7.50 avec un HCO3 de 16 – 18 mEq/L; le changement dans le niveau du bicarbonate comprend les changements provoquer par la réaction d’hydrolyse et la compensation rénale
- si la compensation rénale est complète le nouveau pH serait de 7.45 avec un HCO3 de 14 – 16 mEq/L (nécessite plusieurs semaines)
-
ACIDOSE MÉTABOLIQUE
L’acidose métabolique est défine comme étant un taux de HCO3 artériel en-dessous de la limite normale de 22 mEq/L.
Les causes sont multiples. Le taux de HCO3 peut diminuer pour 2 raisons :
- tamponnage suite à une augmentation d’un acide fixe
- toxines (méthanol, acide salycilate, éthylène glycol)
- acide lactique
- corps cétonique (crise de diabète mellitus et respiration exagérée des acides gras)
- défaillance rénale urémique (augmentation du BUN et de la créatinine)
- réduction ou perte du niveau de HCO3
- diarrhée
- acidose tubulaire rénale
- alimentation via TPN (nutrition parentérale)
- acétazolamine
Afin de différencier les 2 types d’acidose métabolique on calcule le trou anionique. Un trou anionique élevé, au-dessus de 20 mmol/L, indique une acidose métabolique avec ajout d’acides fixes. Un trou anionique normal, 8 – 20 mmol/L, indique une acidose métabolique provoqué par une perte de HCO3. À noter que chaque laboratoire peut avoir une valeur différente pour le trou anionique.
En présence d’acidose métabolique la compensation respiratoire se fait rapidement. L’augmentation des ions H+ dans le sang stimule les chémorécepteurs périphériques stimulant ainsi les centres respiratoires et la ventilation.
Évidemment la ventilation peut augmenter jusqu’à un taux maximal. Habituellement quand la compensation est normale et maximisée on observe que les décimaux du pH sont semblables à la PaCO2. Une compensation complète n’est pas observée pour l’acidose métabolique.
Exemple :
Le niveau de HCO3 passe de 24 mEq/L à 15 mEq/L
-
-
- le nouveau pH sans compensation respiratoire avec une PaCO2 40 mmHg serait de 7.20
- avec une compensation respiratoire maximale le nouveau pH serait de 7.30 avec une PaCO2 de 30 mmHg
-
ALCALOSE MÉTABOLIQUE
Une alcalose métabolique est définie comme étant un taux de HCO3 au-dessus de la limite normale de 26 mEq/L.
Les causes sont multiples. Le taux de HCO3 peut augmenter pour 2 raisons :
- augmentation du taux de HCO3
- administration de stéroïdes
- administration de diurétiques
- alimentation via TPN
- administration de HCO3
- administration de citrate (anticoagulant)
- une diminution des protons H+
- vomissements
- lavage gastrique
En présence d’alcalose métabolique la compensation respiratoire ramène le pH à mi-chemin. Donc une compensation complète n’est pas observé. De plus, les observations démontrent que la PaCO2 n’augmente pas plus que 55 – 60 mmHg.
Exemple :
Le niveau de HCO3 passe de 24 mEq/L à 40 mEq/L
-
-
- le nouveau pH sans compensation respiratoire avec une PaCO2 40 mmHg serait de 7.62
- avec une compensation respiratoire maximale le nouveau pH serait de 7.51 avec une PaCO2 de 51 mmHg
-
Maintenant qu’on comprend que les compensations physiologiques qui se font suite à un désésquilibre acido-basique sont habituellement incomplètes, sauf pour l’acidose respiratoire avec une PaCO2 < 60 – 65 mmHg, on peut déduire qu’un pH parfait 7.39 – 7.41 avec 2 déséquilibres indique la présence d’un déséquilibre mixte.
Exemple :
pH 7.41 PaCO2 25 mmHg HCO3 18 mEq/L
Il n’y a aucune compensation ici. Un déséquilibre mixte est présent. Une alcalose respiratoire + acidose métabolique
Partie B : Quelques petits trucs pour compléter l’analyse des gaz du sang
L’analyse de l’oxygénation dissoute
-
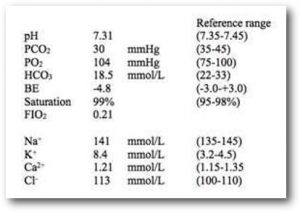
- La PaO2 ne devrait pas surpasser la FiO2 X 5
Exemple :
Patient reçoit une FiO2 de 25%. La PaO2 ne devrait pas surpasser 125 mmHg. Si vous notez que la PaO2 > 125 mmHg une investigation est nécessaire. Donc une erreur est présente : soit une erreur pré-analytique, analytique ou post-analytique.
Pré-analytique : bulle d’air, ponction veineuse, identification du patient, effets métaboliques ou d’anticoagulants
Analytique : bien mélanger l’échantillon, assurer un contrôle de qualité et calibrer la machine
Post-analytique : assurer que la transcription des résultats s’est produit adéquatement
-
- La PaO2 ne devrait pas surpasser 100 mmHg à moins que le patient hyperventile. On peut évaluer la présence d’une hyperventilation facilement en évaluant si la PaCO2 diminuée.
L’analyse acido-basique
-
- On devrait toujours évaluer le trou anionique. Un pH normal n’indique pas toujours une normalité. Il existe parfois 2 déséquilibres métaboliques (acidose métabolique + alcalose métabolique) résultant en un pH normal.
- Analyser les relations entre le pH – PCO2 – HCO3. Par exemple, une hypercapnée est associée à une augmentation du HCO3 entraîner par les changements reliés à la réaction d’hydrolyse.
Exemple :
pH 7.28 PaCO2 60 mmHg HCO3 28 mEq/L
Même si l’analyse de base est une acidose respiratoire partiellement compensé on comprend physiologiquement que l’augmentation du HCO3 est uniquement relié à l’augmentation de la PaCO2. Or il n’y a aucune compensation.
En sachant ceci on peut donc présumer qu’une acidose métabolique serait présente dans l’exemple suivant.
Exemple :
pH 7.24 PaCO2 60 mmHg HCO3 24 mEq/L
Le niveau de HCO3 ici est normal ce qui n’est pas l’observation attendue. On présumerait que le niveau de HCO3 devrait être au moins 27-28 mmHg. De plus le niveau du pH devrait être 7.28 avec une PaCO2 de 60 mmHg (0.06 X 2 = 0.12; 7.40 – 0.12 = 7.28).

