9
Unité d’apprentissage 1 : Introduction
Partie A : Classification des groupes d’enfants
Partie B : L’évaluation de l’enfant
Partie C : Le développement pulmonaire foetal
Partie D : Le placenta et la circulation foetale
Unité d’apprentissage 2 : La naissance et l’évaluation du nouveau-né
Partie A : Le travail maternel et l‘évaluation du foetus
Partie B : La réanimation du nouveau-né et la thermorégulation
Partie C : L’évaluation du nouveau-né et les plans d’interventions
Unité d’apprentissage 3 : Les maladies du nouveau-né et de l’enfant
Partie A : Le syndrome de détresse respiratoire
Partie B : L’apnée du prématuré
Partie C : Les complications associées aux traitements de la thérapie respiratoire
Partie D : Les maladies courantes de l’enfant à terme (PPHN, MAS, TTN)
Partie E : Les maladies cardiaques congénitales
Partie F : Les maladies courantes de l’enfant
Unité d’apprentissage 1 : Introduction
Partie A : Classification des groupes d’enfants
En néonatologie et en pédiatrie on doit évaluer rapidement l’âge et le poids de l’enfant afin de déterminer quel type de traitement est adéquat. Pour les nouveau-nés et les bébés on suit les lignes directrices de la néonatologie. Pour les enfants on suit les lignes directrices de la pédiatrie.
Classification des groupes d’enfants
très prématuré : < 32 semaines
prématuré : 32 à 366/7 semaines
nouveau-né à terme ou bébé (neonate or infant) : bébé < 4 semaines d’âge
enfant : 1 mois à ∼ 12 ans
adolescent : observation des signes de la puberté (poils, etc); on traite l’adolescent comme l’adulte
Un bébé ou un enfant qui souffre de maladies cardiopulmonaire décompense très rapidement car leur réserve anatomique et physiologique sont plus petites que l’adulte. On doit reconnaitre les signes d’une détresse cardiopulmonaire rapidement surtout quand le bébé ou l’enfant est entrain de décompenser. Outre l’Académie Américaine pédiatrique décrit les étapes de la réanimation de l’enfant. L’évaluation doit se faire à l’intérieur d’une minute ‘The Golden Minute’. La vie ou la mort en dépend.

Partie B : L’évaluation de l’enfant
Pour assurer que l’équipe médicale évalue correctement l’enfant selon son âge, administre le bon dosage de médicament, choisit adéquatement l’équipement pour l’entretien des voies aériennes et fournit une ventilation mécanique appropriée on doit déterminer le poids de l’enfant. À l’hôpital on peut peser le bébé ou l’enfant directement sur le lit ou un lit chauffant. Si le lit ne permet pas de peser l’enfant on peut utiliser le ruban Broselow.
Les signes vitaux normaux chez les groupes d’enfants
| Poids de l’enfant (kg) | TA systolique | F.C | F.R |
| < 1 | 55 | 160 | 30 – 60 |
| 1 – 2 | 60 | 160 | 30 – 60 |
| 2 – 3 | 62 | 160 | 30 – 60 |
| 3.5 (n.n) | 65 | 150 | 30 – 60 |
| 7.0 (∼ 6 mois) | 95 | 140 | 30 – 60 |
| 10 (∼ 1 an) | 100 | 125 | 24 – 40 |
| 12 – 14 (2 – 3 ans) | 100 | 110 | 24 – 40 |
| 16 – 20 (4 – 6 ans) | 100 | 100 | 22 – 34 |
| 22 – 27 (6 – 8 ans) | 105 | 90 | 18 – 30 |
| > 30 (> 10 ans) | 115 | 80 | 18 – 30 |
Définitions de l’hypotension
< 1 mois < 60 mmHg
1 à 12 mois < 70 mmHg
1 à 10 ans < 70 mmHg + (âge X 2)
> 10 ans < 90 mmHg
Grosseur du tube endotrachéal
Enfant < 1 an
prématuré 2.5 mm à 3.0 mm
nouveau-né 3.0 mm à 3.5 mm
3 – 12 mois grosseur 4.0 mm
Enfant > 1 an
Avec ballonnet (âge/4) + 3.5
Sans ballonnet (âge/4) + 4.0
Profondeur du ETT
3 X grosseur du ETT
Ventilation mécanique
Ventilation minute 100 ml/kg
Vt 4 – 8 ml/kg
PEEP 5 – 10 cmH2O
L’évaluation de l’oxygénation
L’oxymétrie est facile, non-invasive et précise. N’oubliez pas que la courbe de dissociation chez le nouveau-né est déviée vers la gauche par la présence d’une hémoglobine foetale. L’hémoglobine foetale est transformée en hémoglobine adulte à l’intérieur de 6 mois à 1 an. Donc la saturation pour une PaO2 donnée est plus élevée. L’oxymétrie évalue seulement l’hypoxie hypoxémique et non l’hypoxie anémique, circulatoire ou histotoxique.
Pour les bébés et les enfants plus critiques on peut évaluer la PO2 et la PCO2 avec le moniteur transcutané. Une électrode chauffée (40 – 44 degrés) est placée sur la surface de la peau de l’enfant. La région chauffée devient hyperperfusée et nous permet d’évaluer continuellement les gaz sanguins. Cette technique est considérée sécuritaire. Pour prévenir les brûlures on change le site Q2H – Q4H. Nous devons quand même valider la précision des lectures en obtenant un échantillon de sang artériel.
Les sites appropriés pour l’emplacement de l’électrode sont:
- partie supérieure du thorax droite ou gauche (considération des valeurs pré-canalaire et post-canalaire – droite vs gauche)
- abdomen
- cuisses
- partie inférieure du dos
Chez le prématuré et le nouveau-né on peut insérer un cathéter artériel (UAC) ou veineux (UVC) via le cordon ombélical. Les cathéters ombilicaux sont insérés tôt après la naissance. On insère le UAC préférablement dans l’aorte descendante afin de prévenir une diminution du débit sanguin aux organes abdominaux et les tissus périphériques. Le bout du cathéter UAC peut être positionné entre T6 – T9 ou > L1. Il est inséré pour mesurer la pression sanguine et pour prélever des ABG. Le bout du UVC devrait être entre T9 – T10. Il est inséré pour permettre le prélèvement de sang, d’administrer des infusions et mesurer la CVP. Un cathéter en place pour plus que 72 heures augmente les chances d’infection de façon significative.
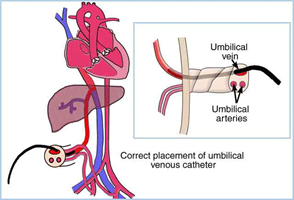
Le cathéter courbé est le UAC.
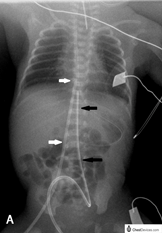
L’analyse des gaz sanguins nécessite un volume de 0.1 – 0.3 mL et donc les erreurs seront plus significatives. De plus, on doit se souvenir que le volume sanguin d’un nouveau-né est seulement de 85 – 90 mL/kg et l’anémie se développera plus rapidement suite à l’échantillonage multiple.
La ponction artérielle (artères radiale, pédieuse, tibiale postérieure, temporale)
La prise de sang est une procédure douloureuse. Chez le nouveau-né on peut tremper la sucette dans une solution de sucrose 24%. Si l’enfant est intubé on administre des gouttes sur la langue ou le palais. Pour les enfants > 4 mois on peut appliquer une crème de lidocaïne ou l’administrer via injection.
La ponction capillaire
On prend du sang artérialisé via le talon qui a été réchauffé pour 5 – 10 minutes avec une débarbouillette chaude. Le sang qui traverse un lit capillaire dilaté ressemble à un échantillon de sang artériel car la diffusion et le mélange des gaz (oxygène et le gaz carbonique) est minimisé. Même si le réchauffement du talon minimise le mélange des gaz du sang on ne prévient pas qu’il y a mélange. C’est pour cette raison qu’on évalue plutôt le pH et la PaCO2 lorsqu’on analyse les résultats de l’échantillonnage capillaire. La PaO2 mesurée est habituellement << de la valeur artérielle.
La radiographie pulmonaire
La radiographie néonatale diffère d’une radiographie pédiatrique ou adulte. Les côtes sont plus horizontales, le diaphragme est plus haut (T8 – T9), le coeur est plus large et peu prendre jusqu’à 60% de la largeur de la cage thoracique.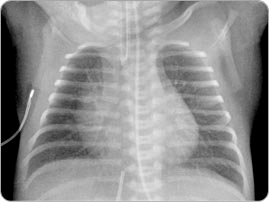
La vue frontale nous permet d’évaluer la position du tube endotrachéal. Le bout du tube doit être situé entre le haut de la cage thoracique et la carène ou entre T2 – T4. La position de la tête impacte significativement la positon du ETT. Un cou en flexion pousse le tube plus creux et l’extension le remonte.
Partie C : Le développement pulmonaire foetal
Le développement pulmonaire foetal
Les poumons se développent pendant les stades embryonnaire et foetal et sont matures seulement autour de la semaine 35 de gestation. Or, tout accouchement prématuré peut mener à des difficultés significatives pour le bébé au niveau de l’échange gazeux. L’âge gestationnel est important à déterminer afin d’estimer la maturation pulmonaire de l’enfant. La précision ultrasonographique du foetus à l’âge de 20 semaines est ± 1 semaine.
Les stades de la grossesse sont classifiés comme suit :
- conception : semaines 1 – 2
- stade embryonnaire : semaines 3 – 12
- stade du développement du foetus : semaine 13 – 41 (287 jours)
L’hypoplasie pulmonaire est caractérisée par un développement immature du système respiratoire. L’hypoplasie pulmonaire peut être causée par un accouchement prématuré, une compression du tissu pulmonaire, un manque de liquide amniotique (oligohydramnios) et certains déséquilibres hormonaux.
L’accouchement prématuré est souvent sans cause. Par contre plusieurs facteurs de risques ont été identifiés.
- diabète
- cigarette
- alcool
- anomalies utérines
- trauma
- stress
- hypo ou hypertension
- autres
Le système pulmonaire foetal se développe comme suit :
- stade embryonnaire
- bourgeonnement des poumons à partir du pharynx 21 – 26 jours après la conception
- le diaphragme se forme 31 jours – 7 semaines
- certaines anormalités congénitales se développent dans ce stade
- atrésie oesophagienne si la trachée et l’oesophage ne se sont pas séparés
- hernie diaphragmatique si le diaphragme ne s’est pas complètement fermé
- phase pseudoglandulaire
- présence de subdivisions bronchiques (4) à partir de la semaine 7 et entre les semaines 10 – 24; on note la présence des subdivisions segmentaires
- développement de l’épithélium, du muscle lisse, des glandes et du cartilage
- présence de mucus à partir de la semaine 13
- une membrane entre l’oropharynx et le nasopharynx se désintègre; l’atrésie des choanes est une anomalie congénitale présente à la naissance si cette membrane est encore présente
- Phase canaliculaire
- semaines 17 – 26 qui permet la survie de l’enfant qui nait prématurément (> 23 – 24 semaines de gestation)
- les bronchioles se multiplient et la vascularisation pulmonaire se développe
- les cellules épithéliales se différencient en cellules type 1 et 2 et sécrètent le fluide pulmonaire foetal afin de maintenir les petites bronchioles ouvertes ; le pH du fluide pulmonaire est plus acide comparativement au fluide amniotique; le fluide monte dans les voies respiratoires, est avalé ou expulsé par la voie orale et se mélange avec le liquide amniotique
- un surfactant immature est retrouvé dans les alvéoles à la semaine 24; ce surfactant est moins stable et est inhibé par l’hypoxie, l’hyperthermie et l’acidose
- Phase sacculaire
- les alvéoles apparaissent autour de la semaine 30
- la présence suffisante de phosphatidylglycérol (PG) est observé à la semaine 35 indiquant que le surfactant est mature
- cliniquement un surfactant mature est mesuré en évaluant
- le rapport lécithine : sphingomyéline (L : S = 2 : 1)
- la présence de PG
- en faisant le ‘foam test’
- en évaluant la concentration des corps lamellaire
- Phase alvéolaire
- le début de cette phase est à la semaine 36
- 15 – 20% des alvéoles sont formées à la naissance (20 – 150 millions)
- la prolifération des alvéoles commence à diminuer après l’âge de 1 – 2 ans mais continue jusqu’à l’âge de 8 ans

Lorsque l’équipe médicale doit arrêter ou anticiper que la mère va accoucher prématurément elle peut administrer des médicaments pour arrêter le travail et accélérer la maturation pulmonaire. Elle peut aussi prélever du fluide pulmonaire afin d’évaluer la maturation pulmonaire du foetus.
Les tocolytiques et les stéroïdes
Un tocolytique est un médicament qui diminue les contractions utérines
- les béta 2 (terbutaline, rifodrine, fénotérol)
- les bloqueurs des canaux calciques (nifédipine)
- les antagonistes à l’ocytocine (atosiban)
- le sulfate de magnésium
- les inhibiteur des prostaglandines (indométhacine)
On ajoute un stéroïde avec le tocolytique pour accélérer la maturation pulmonaire
- bétaméthasone
- dexaméthasone
Partie D : Le placenta et la circulation foetale
Le placenta
Les poumons sont non fonctionnels avant la naissance. Le placenta est l’organe d’échange gazeux entre le foetus et la mère. Il assume le rôle des poumons, du foie et des reins. Le placenta relie physiquement et biologiquement l’embryon à la paroi utérine. Il apparait au 5ième jour après la fécondation et est complètement formé au 5ième mois de grossesse. Le placenta est habituellement placé au niveau supérieur ou latérial dans l’utérus.
Le placenta apporte les nutriments et l’oxygène à l’embryon et au foetus. Il lui débarrasse du gaz carbonique et des déchets métaboliques. Il laisse passer des anticorps maternels pour lui donner une défense immunitaire avant que le système immunitaire se développe. Il assure une certaine protection contre les toxines et les microorganismes. Par contre certaines substances de petits poids moléculaires ou qui sont très solubles peuvent traverser le placenta tels l’alcool, certaines drogues, certains métaux et certains microorganismes.
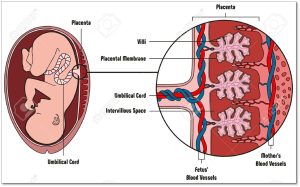
Certaines anomalies qui affectent le placenta
Placenta praevia
- placé au niveau latéro-inférieur (lorsqu’il affleure le bord du col/cervix) ou placé au niveau inférieur dans l’utérus
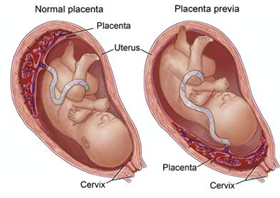
- la mère peut souffrir de saignements durant le 3ième trimestre de la grossesse
- si le placenta est situé entre le foetus et le col, l’accouchement doit se faire via une césarienne
Placenta abruptio
- lorsque le placenta se décolle de l’utérus
- se produit le plus souvent autour de la semaine 25 de gestation mais la cause est souvent inconnue
- les complications maternelles
- choc cardiovasculaire
- problèmes de coagulation
- les complications foetales
- croissance retardée (IUGR)
- naissance prématurée
- mortinaissance

Rupture prématurée des membranes (PROM et PPROM)
- rupture du sac amniotique avant l’accouchement
- si la rupture se poursuit < 37 semaines de gestation on le classifie comme étant une rupture prématuré des membranes (PPROM)
- la rupture peut être associé à ces complications
- accouchement prématuré
- compression avec la corde ombilicale
- infection
- hypoplasie pulmonaire si associé chez le foetus prématuré
- le plan de traitements dépend de l’âge gestationnel

- > 34 semaines
- l’équipe provoque l’accouchement
- administration d’antibiotiques si la mère est Streptococcus B +(GBS)
- 24 – 33 semaines
- tocolytiques + stéroïdes
- antibiotiques si GBS
- < 24 semaines
- discussion avec parents et observation
- > 34 semaines
Oligohydramnios et polyhydramnios
- l’olygohydramnios est défini comme étant une diminution du montant du liquide amniotique
- causé par une rupture prématuré des membranes, un accouchement retardé, des anomalies foetales, l’hypertension maternelle, la diabète, certains médicaments et des anomalies placentaires
- les complications qui peuvent affecter le foetus sont :
- un retard de croissance foetal (IUGR)
- une compression du cordon ombilical
- oligohydramnios
- un accouchement prématuré
Polyhydramnios ou hydramnios
- la polyhydramnios est définie comme étant une augmentation du montant du liquide amniotique
- les causes sont mal connues par contre la polyhydramnios est associée avec :
- anomalies gastro-intestinale chez le foetus comme l’atrésie oesophagienne ou duodénale
- anencéphalie
- fente faciale
- masses au niveau du cou
- fistule trachéo-oesophagienne
- hernie diaphragmatique
La circulation foetale
La circulation foetale est adaptée pour assurer une diffusion entre le foetus et la mêre via le placenta et des poumons qui sont en développement. Le placenta et une oxygénation basse dans les poumons résultent aux déviations de la circulation sanguine à travers des shunts droite et gauche caractérisant la circulation foetale. Le placenta reçoit environ 40% du débit cardiaque foetal tandis que les poumons en reçoit seulement 10%. Or le restant circule à travers les vaisseux sanguins du foetus.
La veine ombilicale est une veine qui transporte le sang oxygéné du placenta vers le foetus. Elle se divise en 2, une partie qui achemine le sang au foie et l’autre partie qui achemine le sang dans le veine cave inférieure par le canal veineux. Deux artères ombilicales transportent le sang désoxygéné du foetus vers le placenta. 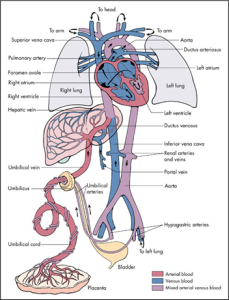
Les poumons étant non fonctionnels chez le foetus seulement 10% de la circulation s’y rend. Les shunts droite-gauche permettent cette déviation.
- le foramen ovale (une partie de la circulation passe de l’oreillette droite à l’oreillette gauche)
- le canal artériel (une partie de la circulation passe de l’artère pulmonaire à l’aorte)
À la naissance voici les changements au niveau de la circulation foetale
- Évacuation du liquide pulmonaire
- pendant le travail et l’accouchement, l’adrénaline foetale est relâchée et cause les cellules type 2 de réabsorber le fluide pulmonaire
- la majorité du fluide pulmonaire est ensuite évacuée pendant l’accouchement par le serrement du thorax dans le canal vaginal
- Les premières respirations sont stimulés par :
- lorsque bébé devient isoler dans le canal artériel, la PO2 baisse qui stimule les chémorécepteurs périphériques et la ventilation
- les changements de l’environnement (environnement noir à une chambre lumineuse, bruyante et froide) et le stimulus physique stimulent les premiers pleurs du bébé
- une pression de 100 cmH2O doit être générée pour ouvrir les alvéoles
- Changements circulatoires
- une fois le cordon ombilical coupé, le placenta est retiré de la circulation néonatale provoquant une augmentation de la pression sanguine systémique du bébé et en même temps, les premières respirations augmentent la PaO2 causant une diminution de la résistance vasculaire pulmonaire.
- Voici les changements qui suivent :
- le retour veineux dans l’oreillette gauche augmente et ferme mécaniquement le foramen ovale
- le shunting droite à gauche à travers le canal artériel est réduit
- l’augmentation de la PaO2 inhibe la production de prostaglandines agissant sur les muscles du canal artériel; alors une vasoconstriction se produit et le canal se ferme; le canal se ferme fonctionnellement environ 12 heures post naisssance et de façon anatomique 2 – 3 semaines post naissance
- les artères et la veine ombilicales vont devenir des ligaments dans les mois suivants la naissance
- Voici les changements qui suivent :
- une fois le cordon ombilical coupé, le placenta est retiré de la circulation néonatale provoquant une augmentation de la pression sanguine systémique du bébé et en même temps, les premières respirations augmentent la PaO2 causant une diminution de la résistance vasculaire pulmonaire.
Unité d’apprentissage 2 – La naissance et l’évaluation du nouveau-né
Partie A : Le travail maternel et l’évaluation du foetus
L’accouchement est divisé en 3; la dilatation du col, l’accouchement et l’expulsion du placenta.
- dilatation du col
- le col est habituellement 4 cm de longueur
- au fur et à mesure que le bébé descend le col raccourci puis s’efface complètement et commence à s’ouvrir
- la dilatation complète du col est atteinte à 10 cm (12 – 25 heures)
- l’accouchement
- la transition entre la vie utérine et la vie extra utérine nécessite habituellement 1 – 2 heures
- le cordon ombilical est coupé après l’accouchement; aujourd’hui on ne coupe pas le cordon immédiatement après la naisssance
- l’expulsion du placenta
- l’expulsion du placenta nécessite environ 30 minutes
L’évaluation du foetus pendant le travail
Deux méthodes sont utilisées pour évaluer le foetus : l’évaluation du rythme et du pouls foetale et le prélèvement de sang du cuir chevelu.
L’évaluation du pouls et du rythme foetal
L’étude du pouls et du rythme cardiaque fœtale est possible avec l’echographie doppler. Le pouls foetal est normalement entre 120 et 160/min. Le but d’évaluer le pouls et le rythme foetal est d’assurer que le foetus demeure stable pendant le travail. Pendant les contractions utérines l’hypoxémie et l’hypoxie qui peut se produire chez le foetus est associé avec des changements cardiaques tels une décélération cardiaque. Si le foetus souffre d’une détresse plus sérieuse on peut le détecter en évaluant les changements cardiaques. Une détresse cardiaque peut être reliée à des causes maternelles ou reliés à des causes foetales.
Causes maternelles
- pathologies chroniques cardiopulmonaires
- l’acidocétose
- compression de l’aorte causé par les contractions utérines
- hypotension
- analgésie péridurale
Causes foetales
- compression du cordon
- infections materno-foetale
- anémie sévère
- décompensation foetale chronique
Voici le vocabulaire associé à l’évaluation du rythme et du pouls foetale
- tachycardie isolée > 180 bpm
- bradycardie < 100 bpm
- décélération précoce (diminution de la F.C foetale avant/pendant les contractions utérines)
- décélérations variables modérés (décélération variable est une diminution de la F.C foetale qui ne correspond pas avec les contractions utérienes)
- amplitude < 50 bpm
- durée > 3.0 < 6.0 secondes
- décélérations variables graves
- amplitude > 50 bpm
- durée > 6.0 secondes
- décélérations tardives
- décalage > 20 secondes par rapport à la contraction utérine
- tracé plats isolés (variabilité < 5.0 secondes)
Une variabilité considérée normale
- accélération du pouls entre 6 – 25 bpm.; cette tachycardie est associée avec les mouvements foetaux
- une décélération précoce et/ou une décélération variable d’une durée < 6.0 secondes est normale
Une variabilité considérée anormale
- une bradycardie persistante
- une décélération variable > 60 secondes
- décélérations tardives répétées (la variation du rythme foetal se produit après les contractions utérines)
- rythme cardiaque foetal sinusoïdal
- tracé plat
Le prélèvement de sang du cuir chevelu
L’échantillonnage de sang du cuir chevelu est utilisé lorsque le monitorage cardiaque n’est pas fiable. Le sang est prélevé du cuir chevelu après que les membranes ont rompues. Le pH sanguin est évalué. Un pH normal est > 7.25.
Partie B : La réanimation du nouveau-né et la thermorégulation
À la naissance environ 10% des bébés nécessitent une réanimation. Le C-A-B pour l’adulte et l’enfant devient A-B-C-T pour le bébé.
Les A-B-C-T pour la réanimation du bébé
- A – airway
- B – breathing
- C – circulation
- T – thermoregulation
La physiologie de la thermorégulation
Un bébé, surtout le prématuré, est à risque d’hypothermie. Un stress causé par un environnement froid augmente le métabolisme et la consommation d’oxygène du bébé et diminue l’efficacité de la réanimation.
Les facteurs suivants augmentent le risque d’hypothermie chez le prématuré :
- la peau est mince et perméable qui augmente la perte de chaleur
- la couche de graisse sous-cutanée est moins étendue et donc le bébé est moins isolé
- le bébé ne peut pas frissonner
- la proportion de graisse brune > la proportion de graisse blanche; cette graisse brune, activée par le froid, est en plus grande proportion chez les bébés et les animaux qui hibernent car les adipocytes présentes peuvent produire de la chaleur par le mécanisme de thermogénèse; la production de chaleur par ce mécanisme est quand même limitée
- le système nerveux est immature et la régulation de l’oxydation des graisses brunes est plus difficile
- le rapport surface : masse corporelle est plus grande chez le bébé surtout le prématuré; le résultat est une perte de chaleur par unité de surface plus grande et un taux métabolique plus élevé
Les complications de l’hypothermie sont :
- hypoxémie
- détresse respiratoire
- apnée
- acidose métabolique
- hyperglycémie, suivit d’une hypoglycémie
- choc
- désordre de coagulation
- mort
Les mécanismes de pertes de chaleur sont :
- la radiation qui permet le transfert de chaleur d’une surface chaude à l’environnement froid
- l’évaporation qui correspond à une perte de chaleur lorsque l’eau à la surface de la peau passe de l’état liquide à l’état de vapeur
- la conduction qui cause le transfert de chaleur directe d’une surface chaude à une surface froide
- la convection qui est associée à la perte de chaleur par un courant d’air
Techniques de prévention de la chaleur chez le nouveau-né
-
- augmenter la température de la salle de réanimation à 26 degrés celcius
- immédiatment après la naissance donner le bébé à la mère pour contact peau à peau
- sécher le bébé naissant
- sécher la tête et mettre un bonnet
- placer le bébé sur un lit chauffant
- mettre le nouveau-né < 32 semaines sur un coussin chauffant
- placé le nouveau-né < 32 semaines dans un sac de polyéthylène
- quand le bébé naissant est stabilité le placer dans un incubateur
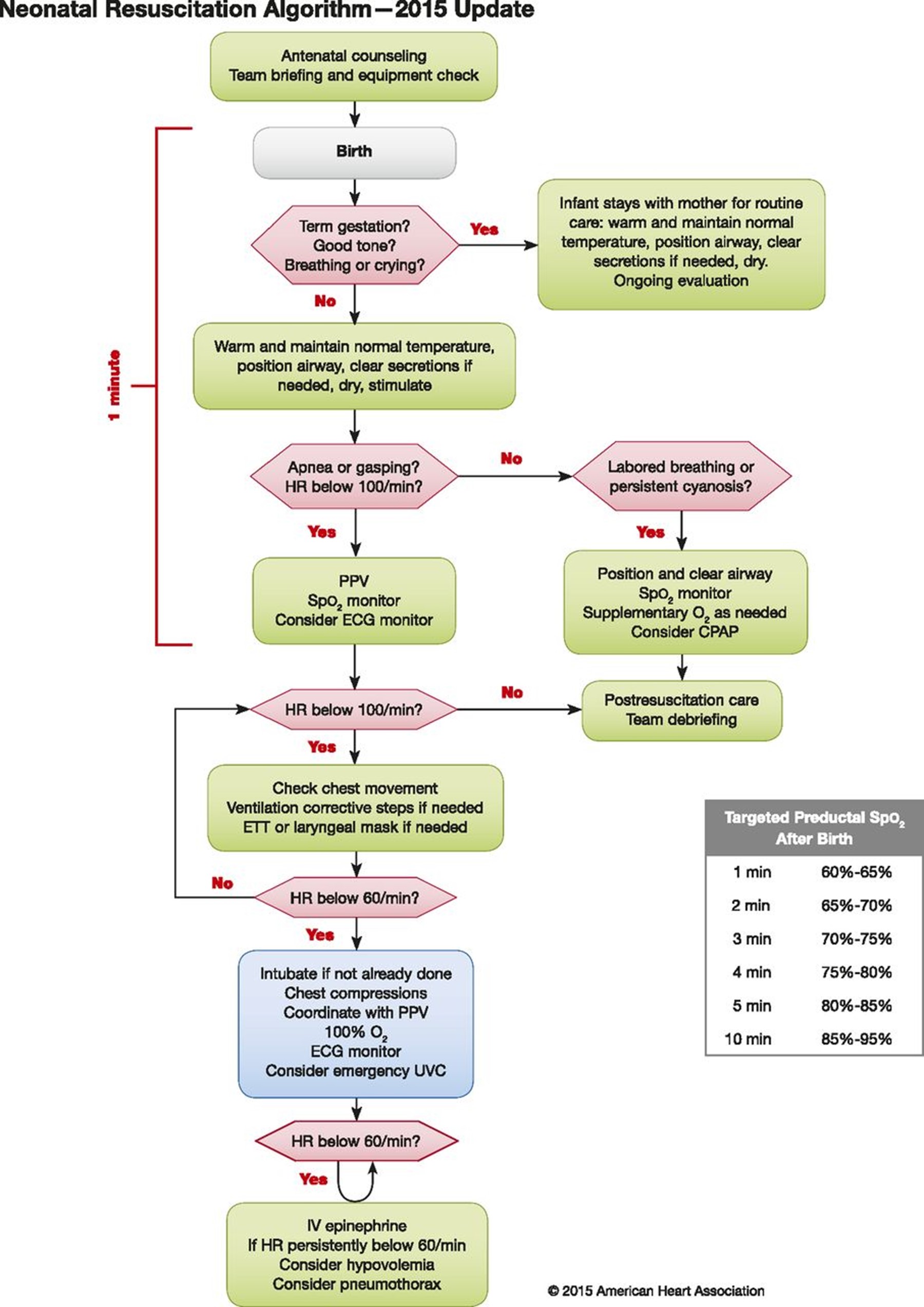
L’évaluation initiale du nouveau-né et les interventions post naissance (the Golden minute)
Questions à se poser avant ou immédiatement après la naissane
- quel est l’âge gestationnel du nouveau-né?
- est-ce que le liquide amniotique est clair?
- quels sont les facteurs de risques : hernie diaphragmatique, oligohydramnios, etc?
- quel est le plan d’action pour le cordon ombilical – couper le cordon ou retarder de couper le cordon?
Plan général de soins : réchauffé, séché, stimulé, ouvrir les voies aériennes, succionner au besoin
À l’intérieur de 30 – 60 secondes après la naissance on évalue l’apparence générale, les pleurs et le tonus musculaire du bébé pour déterminer le plan d’action.
Si le bébé est vigoureux on le sèche et le donne à la mère. On le succionne au besoin (bouche ensuite le nez).
Si le bébé est non vigoureux et > 32 semaines on le sèche, on coupe le cordon à l’intérieur de 30 secondes, on l’amène au lit chauffant, le stimule, le postionne dans la position de renifflement et le succionne au besoin.
Si le bébé est non vigoureux et < 32 semaines on le sèche, on coupe le cordon ombilical à l’intérieur de 30 secondes, le place sur un coussin chauffant sur le lit chauffant, le place dans le sac de polyéthylène, on sèche la tête et lui mets un bonnet, on le positionne dans la position de renifflement et le succionne au besoin.
Partie C : L’évaluation du nouveau-né et les plans d’interventions
Pendant la réanimation on évalue le nouveau né pour déterminer les plans de traitements et on évalue le score APGAR. Ce système de pointage décris l’état du nouveau-né à 1 minute, à 5 minutes et à 10 minutes. L’évaluation peut se poursuivre à chaque 5 minutes jusqu’à ce que la valeur soit égale à 7. L’APGAR est documenté dans le dossier du patient avec les traitements administrés. Si le pointage est entre 1 – 3 les chances que le bébé subit des séquelles neurologiques sont augmentées.

D’autres systèmes de pointage existent et utilisés pour diriger les plans de soins. Le système ACoRN est un système de pointage populaire. Ce système évalue plutôt les signes reliés au système cardiopulmonaire.
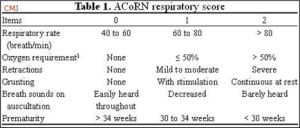
Le pointage guide les plans de soins respiratoires
- détresse légère < 5
- surveillance accrue ou canule nasale si nécessaire
- détresse modéré 5 – 8
- NCPAP ou NIPPV
- détresse sévère ≥ 8
- intubation et ventilation mécanique
- suivre le protocole de l’institution pour l’administration du surfactant
Unité d’apprentissage 3 : Les maladies du nouveau-né et de l’enfant
Partie A : Le syndrome de détresse respiratoire
Les bébés prématurés sont le groupe d’enfants qui nécessitent le plus de soins cardiorespiratoires. L’âge gestationnelle réduite et un petit poids (VLBW 1000 – 1500 grammes ou ELBW 500 – 1 500 grammes) contribuent au développement du syndrome de détresse respiratoire. Cette condition est caractérisée par une hypoplasie pulmonaire et du surfactant immature. Le syndrome de détresse respiratoire est la cause qui contribue à la mortalité élevée chez les prématurés.
La physiopathologie est caractérisée par :
- un manque de surfactant mature
- une compliance pulmonaire réduite
- une compliance thoracique augmentée diminuant l’efficacité de la ventilation
- une augmentation de l’épaisseur de la membrane alvéolo-capillaire
- une hypoplasie pulmonaire
Les nouvelles thérapies, surtout l’administration des stéroïdes à la mère avant la naissance d’un bébé prématuré, a diminué drastiquement la mortalité de cette population (jusqu’à 35%).
La présentation clinique du syndrome
- tachypnée / apnée
- rétractions intercostales
- rétraction sternale
- battements des ailes du nez
- geignements ‘grunting’
- asynchronie abdomino-thoracique (‘see – saw’ breathing pattern)
- hypoxémie
- hypercapnie
- cyanose
- Radiographie : hypoinflation, atélectasie et oedème pulmonaire (bronchogrammes aériens), patron granulaire diffus (ground glass)
Les traitements sont dirigés avec le pointage ACoRN ou par un autre système similaire de pointage. Par exemple, avec le système ACoRN les plans de traitements sont dirigés comme suit:
- détresse légère < 5
- surveillance accrue ou canule nasale si nécessaire
- détresse modéré 5 – 8
- NCPAP ou NIPPV
- détresse sévère ≥ 8
- intubation et ventilation mécanique
- suivre le protocole de l’institution pour l’administration du surfactant
Partie B : L’apnée du prématuré
L’apnée primaire du prématuré contribue aussi à la mortalité du prématuré. Les épisodes d’apnée sont plus fréquentes chez les grands prématurés et les prématurés.
Voici les pourcentages des épisodes d’apnée associé à l’âge gestationnel du bébé :
- 34 – 35 semaines – 7%
- 32 – 33 semaines – 14%
- 30 – 31 semaines – 54%
- en-dessous de 30 semaines – 80%
La bradycardie et l’hypoxémie sont associées avec l’apnée définie par une absence de la respiration pour > 20 secondes. Une période d’apnée sévère ‘spell’ est définie par une absence de la respiration pour au moins 30 secondes accompagnée d’une bradycardie de 50-60/min. pour au moins 10 secondes. À noter que l’apnée du prématuré peut persister chez un enfant âgé plus de 37 semaines mais né prématurément avant l’âge de 28 semaines. Les épisodes sévères cessent habituellement lorsque l’enfant est de 43 semaines.
Les étiologies de l’apnée du prématuré sont l’immaturité des centres respiratoires, l’immaturité des récepteurs et l’obstruction des voies aériennes. D’autres étiologies sont l’infection, une physiopathologie cardiopulmonaire, une hémmoragie cérébrale, un reflux oesophagien, des déséquilibres glycémiques et électrolytiques, l’hypo. et l’hyperthermie et la manipulation.
Les traitements :
- stimulation tactile
- la ventilation manuelle
- la pharmacothérapie – méthylxanthines (caféine)
- transfusions sanguines
- canule nasale
- ventilation non-invasive
- ventilation invasive
- positionnement et stimulation kinesthésique
Partie C : Les complications associées aux traitements de la thérapie respiratoire
Comme l’adulte les soins respiratoires peuvent causer des complications chez le bébé et l’enfant. Ces complications sont associées à l’oxygénothérapie et à la ventilation mécanique.
- reflux gastrique, dommage au nez et dessèchement des sécrétions sont des complications associées à la ventilation non-invasive
- hypotension (diminution du retour veineux et du débit cardiaque)
- pneumonie (VAP)
- dysplasie bronchopulmonaire
- interrruption du développement pulmonaire surtout pour les bébés nés entre 23 – 30 gestation
- caractérisé par une hypoplasie pulmonaire associée à l’interruption du développement des bronchioles terminales, des alvéoles et des capillaires
- on observe une hyperplasie des muscles lisses dans les vaisseaux sanguins pulmonaires et les bronchioles
- barotraumatisme (emphysème pulmonaire interstitiel – PIE, pneumothorax, pneumomédiastinum, pneumopéricardium, pneumopéritonium, emphysème sous-cutané)
- PIE est observé surtout chez les petits prématurés ventilés et se développent dans les premières 4 journées suivants la ventilation mécanique
- surdistension et rupture des petites voies aériennes et des alvéoles; l’air devient emprisonné dans l’espace périvasculaire du tissu pulmonaire
- présence de cystes 1 – 4 mm sur la radiographie
- pour les autres fuites d’air, l’air parvient d’une alvéole surdistendue qui rupture et qui dissecte les tissus conjonctifs le long des v.s. et se dirige vers l’hile ensuite vers la plèvre, ou le péricarde, ou les tissus sous-cutanés ou le péritoine
- l’hémorragie intraventriculaire (IVH) et la leucomalacie
- observé chez les petits prématurés
- l’hémorragie est provoquée par la rupture des vaisseaux sanguins de la matrice germinale. Cette matrice est une vascularisation cérébrale retrouvée chez le foetus entre 20 – 32 semaines permettant une circulation supplémentaire pendant le développent du tissu nerveux
- lorsqu’un bébé nait prématurément, les vaisseaux sanguins cérébraux sont très délicats et peuvent rupturer facilement (matrice germinale) surtout lorsque le débit sanguin cérébral varie rapidement. L’autorégulation de la perfusion cérébrale n’est pas encore fonctionnelle chez ces bébés; les conditions qui peuvent causer des variations dans la perfusion cérébrale sont : la septicémie, un canal artériel persistant (PDA), des changements du volume sanguin, hypo-hypercapnée, hypoxémie, acidose, etc.
- la leucomalacie associée à l’hémorragie intraventriculaire est provoquée par le processus inflammatoire localisé qui cause des lésions et la destruction de la substance blanche autour des ventricules (germinal matrix)
- la sévérité de l’hémorragie est quantifiée de grade 1 étant le moins sévère au grade 4 étant le plus sévère.
- la persistance du canal artériel (PDA)
- un PDA s’observe chez 30% des bébés < 1500 grammes et 70% < 1000 grammes possiblement à cause d’une PaO2 basse
- la présence de RDS et la prématurité augmente significativement les risques
- l’entérocolite nécrosante (NEC)
- observé chez les prématurés
- l’ischémie et l’hypoxie provoquent un processus inflammatoire des tissus digestifs qui peut résulter en la mort tissulaire
- les bébés qui développent NEC peuvent nécessiter l’assistance respiratoire suite à l’augmentation des périodes d’apnée, l’oedème pulmonaire et la réduction de la compliance thoracique
- la rétinophathie du prématuré (ROP – toxicité d’oxygène)
- désordre qui affecte la prolifération vasculaire de la rétine chez les prématurés
- l’environnement hyperoxique extra-utérine dérange et abolit le développement des vaisseaux sanguins de la rétine
Partie D : Les maladies courantes de l’enfant à terme (PPHN, MAS, TTN)
| Physiopathologie | Manifestations cliniques | Traitements |
| L’hypertension persistante du nouveau-né (PPHN)
Incapacité à la circulation foetale de faire la transition à la circulation extra-utérine |
cyanose progressive après la naissance
différence des SpO2 pré-canalisation et post-canalisation > 10% Index d’oxygénation > 20 test d’hyperoxie pour évaluer si la cause est d’origine respiratoire ou cardiaque |
oxygénothérapie et ventilation mécanique HFV, surfactant, ECMO vasodilatateurs (NO, sildenafil, prostacycline) MgSO4 milrinone |
| Le syndrome de l’aspiration de méconium (MAS)
Inhalation de méconium intra ou extra-utéro Obstruction aérienne qui peut causer effet ‘one way valve ou ball-valve’ et causer l’entrappement d’air Oedème et possiblement hémorragie pulmonaire Hypertension pulmonaire Altération du surfactant
|
cyanose
crépitements fins et/ou gras, sibilances radiographie : infiltrats, patron réticulaire, atélectasie avec zones d’hyperinflation, pneumothorax si présent |
oxygénothérapie, ventilation mécanique – HFV si possible
surfactant NO ECMO |
| Tachypnée transitoire du nouveau-né (TTN)
Diminution de la résorption du liquide foetal pendant le travail et/ou diminution de l’évacuation du liquide foetal pendant le passage dans le col |
augmentation du travail respiratoire qui se présente à l’intérieur des premières 6 heures suivant l’accouchement radiographie : infiltrats diffus et/ou accumulation de fluide interstitiel si après 72 heures le bébé nécessite une FiO2 > 0.40 un autre diagnostic doit être établi |
oxygénothérapie
Ncpap 4 – 6 cmH2O |
Partie E : Les maladies cardiaques congénitales
Approximativement 1% des enfants souffrent de maladies cardiaques congénitales qui sont habituellement causées par des anomalies génétiques. Ces maladies sont classifiées en 2 groupes : les maladies cardiaques qui ne sont pas associées à la cyanose et les maladies cardiaques qui sont associées à la cyanose.
Types de shunting
Les maladies cardiaques congénitales qui ne sont pas associées à la cyanose sont caractérisées par des shunts gauche – droit
Les maladies cardiaques congénitales qui sont associées à la cyanose sont caractérisées par des shunt droit – gauche
Le diagnostic se fait habituellement avant la naissance avec l’ultrason. Pour les enfants qui n’ont pas été diagnostiqués avant la naissance les tests suivants peuvent confirmer la présence d’une anomalie : ECG, radiographie, echocardiographie, echocardiographie avec doppler, auscultation.
Les défectuosités cardiaques sans cyanose
- anomalies du septum auriculaire ou ventriculaire
- sténose aortique
- sténose de l’artère pulmonaire
- coarctation de l’aorte
- double arque aortique
Ces anomalies sont habituellement associé avec une circulation pulmonaire augmenté qui est causée par le shunt gauche – droit.
Les manifestations cliniques sont :
- aymptomatique
- fatigue
- intolérance à l’exercice
- gain de poids insuffisant
- tachypnée
- murmure
- CHF (peu fréquent)
Les défectuosités cardiaques avec cyanose 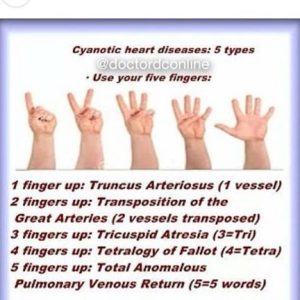
- tétralogie de Fallot (botte ou sabot sur la radiographie)
- anomalie du retour veineux
- transposition des gros vaisseaux
- hypoplasie du ventricule gauche
- anomalie Ebstein
- truncus arteriosus
Les maladies congénitales cardiaques qui causent de la cyanose résultent par le shunting de sang désoxygéné avec le sang oxygéné. Les bébés dont la saturation d’oxygène n’est que 85 – 90% même avec de l’oxygénothérapie doivent être évalués pour ce type d’anormalité. Le test d’hyperoxie peut aider à déterminer si l’hypoxémie réfractaire est causé par un désordre pulmonaire (PPHN) ou un désordre cardiaque.
Il est aussi possible de déceler des anomalies congénitale à l’aide de la radiographie pulmonaire. Grâce à la vue de la silhouette cardiaque, il est possible de cibler un désordre, même si d’autres tests plus précis sont nécessaire pour déterminer le diagnostique officiel.
Tétralogie de fallot: Coeur en silhouette de sabot
Anomalie du retour veineux: Coeur en silhouette de bonhomme de neige
Anomalie de Ebstein: Coeur en silhouette sphérique
Transposition des gros vaisseaux: Coeur en silhouette d’oeuf
Le test d’hyperoxie
- on retire 2 échantillons artériels par l’artère radiale droite
- le premier sur l’air ambiant et le second sur 100% pour une durée de 10 – 15 minutes (oxyhood ou masque)
- si la PaO2 sur 100% est supérieure à 150 mmHg l’étiologie de l’hypoxémie est probablement causée par un désordre pulmonaire; si la PaO2 est en-dessous de 150 mmHg l’étiologie de l’hypoxémie est possiblement causé par une maladie congénitale cardiaque associée à la cyanose
Partie F : Les maladies courantes de l’enfant
Cette partie est divisée en deux :
- les algorithmes de l’arrêt cardiorespiratoire, la tachycardie et la bradycardie
- les pathologies affectant les voies aériennes et le parenchyme pulmonaire
Les algorithmes
L’arrêt cardiorespiratoire
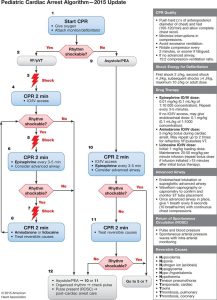
La tachycardie
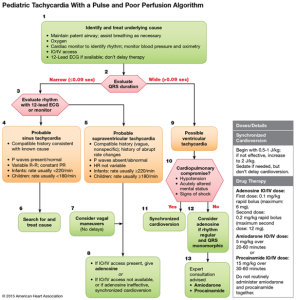
La bradycardie
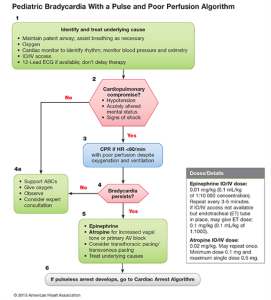
Les pathologies affectant les voies aériennes et le parenchyme pulmonaire
Croupe (laryngotrachéobronchite)
- infection virale affectant la région sous-glottique
- affecte surtout les enfants entre 6 mois – 3 ans
- toux aboyante, voix rauque, stridor, augmentation du travail resp., fièvre légère, signe de clocher ‘steeple’ sur la radiographie
- oxygène, vaponéphrine (2.25%), stéroïde, HeO2, intubation
Épiglottite
- infection bactérienne affectant la région de l’épiglotte (H. influenzae B, Staphylococcus, Streptococcus)
- affecte surtout les enfants de 2 – 5 ans
- tripode, dysphagie, salivation, dysphonie, stridor, signe du pouce ‘thumb’ sur radiographie latérale
- oxygène, antibiotique, entretien des voies aériennes algorithme difficile qui nécessite spécialistes et anesthésiques
Trachéite bactérienne (croupe bactérienne)
- infection bactérienne affectant la trachée chez les enfants de 6 mois – 8 ans (Staphylococcus, Streptococcus, Haemophilus, Moraxella catarrhalis)
- les signes ressemblent aux signes de croupe et d’épiglottite
- augmentation de la production de mucus épaix et purulent
- plus confortable dans la position couchée comparativement à la croupe et l’épiglottite
- oxygène, hygiène bronchique, antibiotiques, intubation
Bronchiolite
- infection virale le plus souvent causer par le virus syncitial respiratoire (RSV) chez les enfants en-dessous de 1 an
- congestion nasale, toux, augmentation du travail resp., sibilances, crépitements gras
- infiltrats et hyperinflation sur la radiographie
- oxygène, bronchodilatateurs, stéroïdes, vaponéphrine, physiothérapie, succion, salin hypertonique, ventilation non-invasive ou invasive, hydratation, agents antiviraux comme ribavarin
Asthme
- hypersensibilité type 1 avec hyperactivité des voies aériennes associé à l’atopie
- toux, sibilances, diminution de l’entrée d’air
- provocation bronchique (≥ 8 ans) et FENO pour faire le diagnotic
- ICS, SABA, MgSO, HeO2, NIPPV, etc
Fibrose cystique
- désordre génétique qui affecte les canaux de chlore de l’épithélium respiratoire
- accumulation de mucus épaix et visqueux et insuffisance pancréatique
- augmentation des infections pulmonaires (S. aureus, P. aeruginosa)
- malnutrition, sels abondantes et visqueuses (méconium ileus), augmentation des sécrétions respiratoire et sibilances
- taux de sel dans la sueur augmenté et test de sudation pour faire le diagnotstic, test génétique
- bronchodilatateurs, mucolytiques, antibiotiques, enzymes digestives
Pneumonie
- inflammation du tissu pulmonaire par des agents infectieux dont les plus importants sont : S. pneumoniae, S. aureus, Klebsiella, Haemophilus influenzae, Influenze, RSV
- augmentation du travail respiratoire, fièvre (surtout si bactérien)
- cultures et radiographie pour faire le diagnostic
- antibiotiques, antipyrétiques, etc
Atrésie des choanes complète ou incomplète
- anomalie congénitale ou relié à l’hydramnios
- 50% des bébés respirent strictement par le nez; une respiration via la bouche est un signe de détresse grave
- la détresse respiratoire augmente avec les boires et diminue avec les pleures (car respire par la bouche)
- incapacité de passer un cathéter à travers les narines
- ’tissue test’, miroir, endoscopie, tomographie
- sonde oropharyngienne, intubation, chirurgie
Syndrome Pierre-Robin
- anomalie congénitale qui se présente avec une triade qui consiste d’un petit mandibule, une glossoptose et une fente palatine (cleft palate)
- détresse respiratoire causé par la glossoptose, apnée du sommeil obstructive, difficulté avec les boires
- placer le bébé sur le côté ou le ventre, insérer une sonde nasopharyngée et/ou un tube nasogastrique, trachéotomie, chirurgie
Laryngomalacie
- anomalie congénitale, trauma associé à la manipulation du larynx comme l’insertion d’un tube endotrachéal
- si l’anomalie est congénitale un stridor sera entendu environ 2 semaines après la naissance
- stridor, difficulté avec les boires, aspiration, GERD, apnée
- endoscopie pour faire le diagnostic
- position assisse ou de pronation (si l’épiglotte est affectée), intubation, chirurgie
Fistule trachéo-oesophagienne
- associé avec la polyhydramnios
- salivation excessive avec sécrétions mousseuses, toux et étouffement associé avec les boires, infections pulmonaires
- difficulté à insérer un tube nasogastrique, radiographie pour faire le diagnostic
- position 45 degrés, TPN, intubation, chirurgie

