20 Système endocrinien
Objectifs d’apprentissage
- Connaître l’anatomie du système endocrinien.
- Décrire les principales fonctions du système endocrinien.
- Bien orthographier les termes médicaux du système endocrinien et utiliser les bonnes abréviations.
- Nommer les spécialités médicales associées au système endocrinien.
- Explorer les maladies, les troubles et les interventions couramment associés au système endocrinien.
Affixes et radicaux du système endocrinien
Cliquez sur les préfixes, les radicaux et les suffixes pour afficher une liste de composantes de termes à mémoriser pour le système endocrinien.
Un élément interactif ou multimédia a été exclu de cette version du texte. Vous pouvez y accéder en ligne à l’adresse suivante :
https://ecampusontario.pressbooks.pub/medicalterminology/?p=269.
Introduction au système endocrinien
Vous ne l’avez peut-être jamais vu ainsi, mais quand vous envoyez un texto à deux de vos ami.e.s pour les inviter à vous rejoindre à 18 heures à la salle à manger, vous leur envoyez des signaux numériques qui, du moins l’espérez-vous, influenceront leur comportement, même s’ils se trouvent à une certaine distance de vous. De la même façon, certaines cellules envoient à d’autres cellules de l’organisme des signaux chimiques qui influencent leur comportement. Cette communication, coordination et régulation intercellulaire à longue distance est essentielle pour maintenir l’homéostasie, c’est-à-dire l’équilibre du corps. C’est la fonction fondamentale du système endocrinien.
Regardez la vidéo :
Vidéo 20.1. Endocrine System, Part 1 – Glands & Hormones: Crash Course A&P #23 (Système endocrinien, partie 1 – Glandes et hormones : cours accéléré en anatomie et physiologie no 23) [Vidéo en ligne]. © CrashCourse, 2015.
Termes médicaux relatifs au système endocrinien
Un élément interactif ou multimédia a été exclu de cette version du texte. Vous pouvez y accéder en ligne à l’adresse suivante :
https://ecampusontario.pressbooks.pub/medicalterminology/?p=269.
Anatomie (structures) du système endocrinien
Le saviez-vous?
Le pancréas agit comme une glande à la fois endocrine et exocrine.
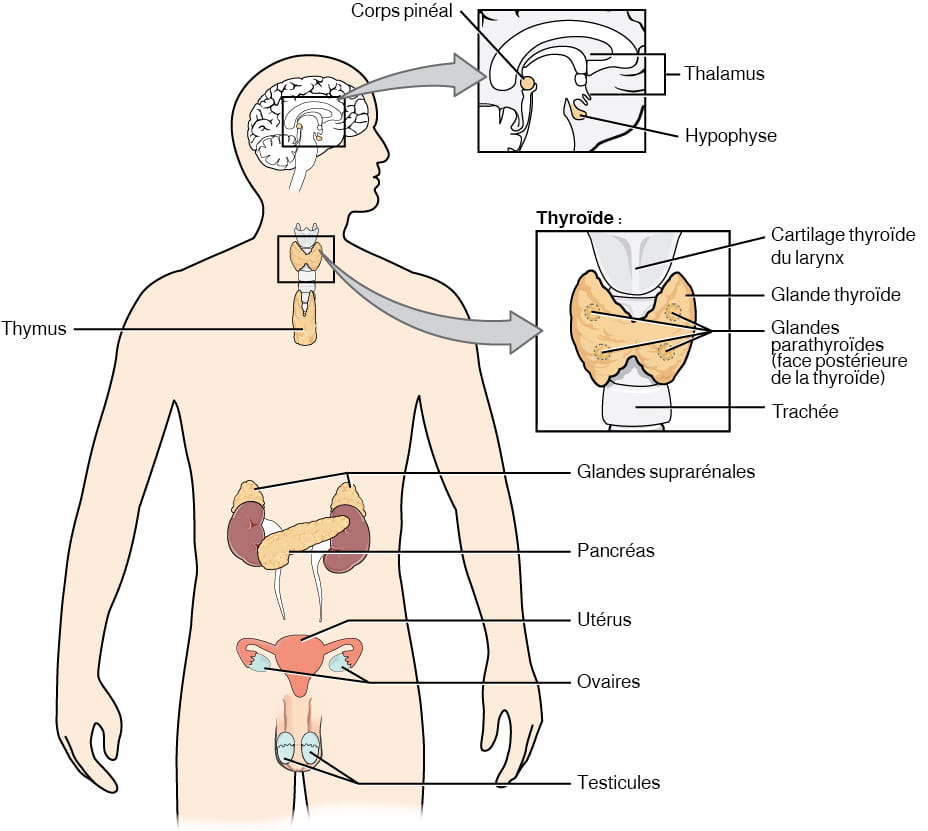
Le système endocrinien est constitué de cellules, de tissus et d’organes dont la fonction primaire ou secondaire est la sécrétion d’hormones. Les glandes endocrines sont les principales intervenantes de ce système. Leur fonction primaire est de sécréter des hormones directement dans le liquide environnant. Le liquide environnant (liquide interstitiel) et les vaisseaux sanguins transportent ensuite les hormones dans tout l’organisme. Le système endocrinien comprend l’hypophyse, le corps pinéal et les glandes thyroïdes, suprarénales (ou surrénales) et parathyroïdes (voir la figure 20.2). Certaines de ces glandes ont des fonctions endocrines et non endocrines. Le pancréas, par exemple, contient des cellules dotées d’une fonction digestive et des cellules qui sécrètent des hormones endocrines comme l’insuline et le glucagon, qui régulent la glycémie (taux de glucose dans le sang). L’hypothalamus, le thymus, le cœur, les reins, l’estomac, l’intestin grêle, le foie, la peau, les ovaires et les testicules contiennent aussi des cellules à fonction endocrine. De plus, on sait depuis longtemps que la graisse (tissu adipeux) produit des hormones et des recherches récentes ont révélé que même le tissu osseux possède des fonctions endocrines.
Il ne faut pas confondre les glandes endocrines sans conduit excréteur avec les glandes du système exocrine de l’organisme, qui elles, libèrent leurs sécrétions par des conduits excréteurs. Les glandes sébacées et sudoripares de la peau sont des exemples de glandes exocrines. Comme mentionné plus haut, le pancréas possède lui aussi une fonction exocrine : la plupart de ses cellules sécrètent du suc pancréatique par les conduits pancréatiques principal et accessoire jusque dans la lumière de l’intestin grêle.
Activité d’identification de l’anatomie
Un élément interactif ou multimédia a été exclu de cette version du texte. Vous pouvez y accéder en ligne à l’adresse suivante :
https://ecampusontario.pressbooks.pub/medicalterminology/?p=269.
Physiologie (fonctions) du système endocrinien
Signalisation endocrine
Le système endocrinien utilise une méthode de communication appelée « signalisation chimique ». Elle désigne l’envoi de signaux chimiques par les organes endocriniens. Les organes endocriniens sécrètent des substances chimiques (les hormones) dans le liquide à l’extérieur des cellules tissulaires (liquide extracellulaire). Les hormones circulent ensuite dans l’ensemble du corps, principalement par la circulation sanguine, pour se lier à des récepteurs sur des cellules cibles, ce qui génère une réponse particulière. Par exemple, la réaction de lutte ou de fuite, qui survient lorsqu’on vit une situation dangereuse ou terrifiante, est déclenchée par la libération en quelques secondes d’hormones provenant des glandes suprarénales (l’épinéphrine et la norépinéphrine, aussi appelées adrénaline et noradrénaline). À l’inverse, la réponse des cellules cibles à certaines hormones de reproduction peut prendre jusqu’à 48 heures.
De plus, la signalisation endocrine est habituellement moins précise que la signalisation neurale (ou nerveuse). Une même hormone peut aussi jouer un rôle dans plusieurs processus physiologiques différents selon les cellules cibles touchées. Par exemple, l’ocytocine (OT) est une hormone qui déclenche des contractions utérines chez les femmes en travail, mais elle est aussi déterminante dans le déclenchement du réflexe d’éjection du lait pendant l’allaitement et peut jouer un rôle dans la réponse sexuelle et les sentiments d’attachement émotionnel chez les hommes et les femmes.
Généralement, le système nerveux réagit rapidement à des changements abrupts dans l’environnement externe, tandis que le système endocrinien opère plus lentement et prend soin de l’environnement interne du corps en maintenant l’équilibre (homéostasie) et en contrôlant la reproduction (voir le tableau 20.1). Dans ce cas, comment se fait-il que la réaction de lutte ou de fuite mentionnée plus tôt se produise aussi rapidement si les hormones qui la provoquent prennent habituellement plus de temps à agir? C’est parce que les deux systèmes sont interreliés. En effet, c’est la réaction rapide du système nerveux au danger dans l’environnement qui stimule les glandes suprarénales, qui à leur tour sécrètent leurs hormones, soit l’épinéphrine et la norépinéphrine. Par conséquent, le système nerveux peut déclencher rapidement des réponses endocrines pour pallier les changements soudains des environnements externes et internes, lorsque la situation l’exige.
| Caractéristique | Système endocrinien | Système nerveux |
|---|---|---|
| Forme(s) de signalisation | Chimique | Chimique et électrique |
| Signal chimique principal | Hormones | Neurotransmetteurs |
| Distance parcourue | Longue ou courte | Toujours courte |
| Temps de réponse | Rapide ou lent | Toujours rapide |
| Environnement(s) ciblé(s) | Interne | Interne et externe |
Autres modes de signalisation chimique
La signalisation chimique dans les organismes multicellulaires se produit selon quatre modes différents : endocrine, autocrine, paracrine et par contact direct.
La signalisation endocrine désigne le fait que les hormones sécrétées dans le liquide extracellulaire se propagent dans le sang ou le système lymphatique et peuvent ainsi parcourir de grandes distances dans l’organisme.
À l’inverse, la signalisation autocrine s’effectue à l’intérieur d’une même cellule. Une substance autocrine (où « auto- » signifie « soi-même ») est une substance chimique qui déclenche une réponse dans la cellule même qui l’a sécrétée. L’interleukine-1 (ou IL-1), par exemple, est une molécule de signalisation chimique qui joue un rôle dans l’inflammation. Les cellules qui libèrent de l’IL-1 possèdent aussi sur leur surface des récepteurs auxquels se lie l’IL-1, ce qui génère une signalisation autocrine.
La signalisation paracrine s’effectue quant à elle entre des cellules avoisinantes. Une sécrétion paracrine (où « para- » signifie « à proximité ») est une substance chimique qui déclenche une réponse dans les cellules voisines. Bien que les sécrétions paracrines puissent passer dans la circulation sanguine, leur concentration est généralement trop faible pour susciter une réponse des tissus distants. L’histamine, une substance paracrine libérée par les cellules immunitaires, est un exemple bien connu des personnes souffrant d’asthme. L’histamine provoque la constriction des cellules musculaires lisses des poumons, ce qui rétrécit les voies respiratoires.
La signalisation par contact direct se produit entre des cellules adjacentes par l’entremise des jonctions communicantes. Les jonctions communicantes sont des canaux qui relient entre elles des cellules voisines, permettant ainsi le passage de petites molécules entre ces cellules.
Vérification des connaissances
- Décrivez les modes de communication utilisés par le système endocrinien.
- Faites la comparaison et la distinction entre les glandes endocrines et exocrines.
- Vrai ou faux : Les neurotransmetteurs représentent une classe particulière de substances paracrines. Justifiez votre réponse.
Hormones
Même si une hormone donnée peut traverser tout l’organisme par la circulation sanguine, elle peut uniquement modifier le fonctionnement de ses cellules cibles, c’est-à-dire celles qui possèdent des récepteurs propres à cette hormone. La liaison de l’hormone au récepteur provoque une chaîne d’événements qui entraîne finalement la réponse de la cellule cible. Les hormones jouent donc un rôle déterminant dans la régulation des processus physiologiques lorsqu’elles génèrent des réponses de leurs cellules cibles, puisque ces réponses favorisent la régulation de nombreuses fonctions de l’organisme, notamment le sommeil, la reproduction humaine, la croissance et le développement des tissus corporels, le métabolisme ainsi que l’équilibre hydroélectrolytique. Les principales hormones du corps humain et leurs effets sont énumérés dans le tableau 20.2.
| Glande endocrine | Hormones associées | Classe chimique | Effet |
|---|---|---|---|
| Hypophyse (antérieure) | Hormone de croissance (GH) | Protéine | Favorise la croissance des tissus corporels |
| Hypophyse (antérieure) | Prolactine (PRL) | Peptide | Favorise la production de lait maternel |
| Hypophyse (antérieure) | Thyréostimuline (TSH) | Glycoprotéine | Stimule la sécrétion d’hormones thyroïdiennes |
| Hypophyse (antérieure) | Hormone adrénocorticotrope (ACTH) | Peptide | Stimule la libération d’hormones par le cortex des glandes suprarénales |
| Hypophyse (antérieure) | Hormone folliculostimulante (FSH) | Glycoprotéine | Stimule la production de gamètes |
| Hypophyse (antérieure) | Hormone lutéinisante (LH) | Glycoprotéine | Stimule la production d’androgènes par les gonades |
| Hypophyse (postérieure) | Hormone antidiurétique (ADH) | Peptide | Stimule la réabsorption de l’eau par les reins |
| Hypophyse (postérieure) | Ocytocine | Peptide | Stimule les contractions utérines pendant l’accouchement |
| Thyroïde | Thyroxine (T4), triiodothyronine (T3) | Amine | Stimule le métabolisme de base |
| Thyroïde | Calcitonine | Peptide | Réduit le taux de Ca2+ dans le sang |
| Parathyroïdes | Hormone parathyroïdienne (PTH) | Peptide | Augmente le taux de Ca2+ dans le sang |
| Glandes suprarénales (cortex) | Aldostérone | Stéroïde | Augmente le taux de Na+ dans le sang |
| Glandes suprarénales (cortex) | Cortisol, corticostérone, cortisone | Stéroïde | Augmente la glycémie |
| Glandes suprarénales (zone médullaire) | Épinéphrine, norépinéphrine | Amine | Stimule la réaction de lutte ou de fuite |
| Corps pinéal | Mélatonine | Amine | Régule les cycles de sommeil |
| Pancréas | Insuline | Protéine | Réduit la glycémie |
| Pancréas | Glucagon | Protéine | Augmente la glycémie |
| Testicules | Testostérone | Stéroïde | Stimule le développement des caractères sexuels secondaires masculins et la production de spermatozoïdes |
| Ovaires | Œstrogènes et progestérone | Stéroïde | Stimule le développement des caractères sexuels secondaires féminins et prépare le corps à l’accouchement |
Types d’hormones
Les hormones du corps humain peuvent être divisées en deux groupes principaux en fonction de leur structure chimique. Les amines, les peptides et les protéines font partie du groupe d’hormones dérivées des acides aminés et les stéroïdes appartiennent au groupe d’hormones dérivées des lipides (voir tableau 20.3). Ces groupes chimiques définissent la distribution de l’hormone, le type de récepteurs auxquels elle se lie et d’autres aspects de sa fonction.
| CLASSE D’HORMONES | COMPOSANTS | EXEMPLES |
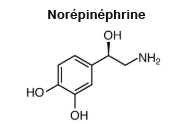
| Hormone amine | Acides aminés dont les groupes sont modifiés (p. ex., le groupe carboxyle de la norépinéphrine est remplacé par un noyau benzénique) |
Structure cellulaire de la norépinéphrine
|
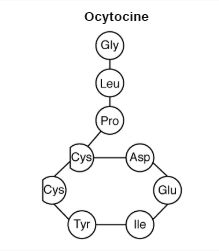
| Hormone peptidique | Courtes chaînes d’acides aminés interreliés |
Structure cellulaire de l’ocytocine
|
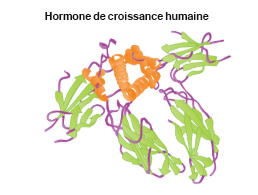
| Hormone protéique | Longues chaînes d’acides aminés interreliés |
Hormone de croissance humaine illustrée
|
| Hormones stéroïdes | Dérivées du cholestérol |
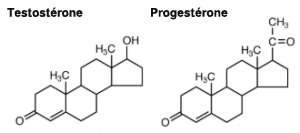
Structure cellulaire de la testostérone et de la progestérone
|
Hormones amines
Les hormones amines sont des hormones dérivées d’acides aminés modifiés. Elles sont synthétisées à partir du tryptophane ou de la tyrosine. La mélatonine, une hormone sécrétée par le corps pinéal qui contribue à réguler le rythme circadien, est un exemple d’hormone dérivée du tryptophane.
Hormones peptidiques et protéiques
Si les hormones amines sont dérivées d’un seul acide aminé, les hormones peptidiques et protéiques sont constituées quant à elles de plusieurs acides aminés interreliés qui forment une chaîne d’acides aminés. L’hormone antidiurétique (ADH), une hormone hypophysaire essentielle au maintien de l’équilibre hydrique, est un exemple d’hormone peptidique, tandis que l’hormone folliculostimulante (FSH) et l’hormone de croissance, produite par l’hypophyse, sont des exemples d’hormones protéiques. La FSH stimule la maturation des ovules dans les ovaires et des spermatozoïdes dans les testicules.
Hormones stéroïdes
Les stéroïdes constituent les principales hormones dérivées des lipides. Les hormones stéroïdes sont dérivées du cholestérol. Les œstrogènes et la testostérone, des hormones de reproduction produites par les gonades (ovaires et testicules), sont des exemples d’hormones stéroïdes. Les glandes suprarénales produisent aussi des hormones stéroïdes, soit l’aldostérone, qui contribue à l’osmorégulation, et le cortisol, qui aide à maintenir le bon fonctionnement du métabolisme.
À l’instar du cholestérol, les hormones stéroïdes ne sont pas solubles dans l’eau; elles sont hydrophobes. Puisque le sang est constitué d’eau, les hormones dérivées des lipides doivent se lier à une protéine de transport pour atteindre leur cellule cible.
Le saviez-vous?
Des chercheurs affirment qu’une semaine de camping sans appareils électroniques peut réinitialiser notre horloge biologique et synchroniser notre production de mélatonine avec le lever et le coucher du soleil (Shurkin, 2013).
Voies hormonales
Le message envoyé par une hormone est reçu par un récepteur hormonal, une protéine située dans la cellule ou dans la membrane cellulaire. Le récepteur traite le message en produisant d’autres signaux ou mécanismes intracellulaires qui aboutissent à la réponse de la cellule cible. Les récepteurs hormonaux reconnaissent les molécules dotées de formes et de chaînes latérales précises et répondent uniquement à ces hormones. Un même type de récepteur peut être fixé à des cellules de différents tissus corporels et déclencher des réponses relativement différentes. La réponse déclenchée par une hormone dépend donc non seulement de l’hormone elle-même, mais aussi de sa cellule cible.
Lorsque la cellule cible reçoit le signal de l’hormone, elle peut répondre de différentes manières : elle peut stimuler la synthèse de protéines, activer ou désactiver les enzymes, altérer la perméabilité de la membrane cellulaire, modifier le rythme de la mitose et de la croissance cellulaire et stimuler la sécrétion de produits. En outre, une seule hormone peut avoir la capacité de provoquer différentes réponses dans une cellule donnée.
Facteurs influençant la réponse d’une cellule cible
Rappelons-nous qu’une cellule cible doit posséder des récepteurs spécifiques à une hormone donnée pour générer une réponse à celle-ci. Toutefois, plusieurs autres facteurs peuvent influencer la réponse d’une cellule cible. Par exemple, si une hormone circule en quantité importante dans le sang, il se peut que ses cellules cibles réduisent leur nombre de récepteurs pour cette hormone. Ce processus appelé « régulation négative » permet aux cellules de réagir moins fortement au taux excessif d’hormones. Lorsque le taux d’une hormone est chroniquement réduit, les cellules cibles amorcent une régulation positive pour augmenter leur nombre de récepteurs, ce qui augmente la sensibilité des cellules à l’hormone en question. Les cellules peuvent également modifier la sensibilité des récepteurs eux-mêmes à différentes hormones.
Deux ou plusieurs hormones peuvent interagir pour influencer de différentes façons la réponse des cellules. Voici les trois types d’interactions les plus courantes :
- L’effet permissif, où la présence d’une hormone permet à une autre hormone d’agir. Par exemple, les hormones thyroïdiennes ont des relations permissives complexes avec certaines hormones de reproduction. Ainsi, une carence alimentaire en iode, l’un des composants des hormones thyroïdiennes, peut avoir un effet sur le développement et le fonctionnement de l’appareil reproducteur.
- L’effet synergique, où deux hormones ayant des effets semblables déclenchent une réponse amplifiée. Dans certains cas, il faut deux hormones pour générer une réponse adéquate. Par exemple, la maturation des ovules nécessite l’intervention de deux hormones de reproduction différentes : la FSH, sécrétée par l’hypophyse, et les œstrogènes, produits par les ovaires.
- L’effet antagoniste, où deux hormones ont des effets opposés. Les effets de deux hormones pancréatiques, soit l’insuline et le glucagon, sont un exemple bien connu. L’insuline augmente les réserves de glucose sous forme de glycogène dans le foie, tandis que le glucagon stimule la dégradation des réserves de glycogène, ce qui augmente la glycémie.
Vérification des connaissances
- Décrivez comment un récepteur hormonal fonctionne et répond aux messages qu’il reçoit.
- Comparez la régulation positive et la régulation négative. Ces processus sont-ils tous deux nécessaires? Pourquoi?
Régulation de la sécrétion hormonale
Afin d’éviter un taux anormal d’hormones et l’apparition potentielle de maladies, il est important de contrôler étroitement son taux d’hormones. L’organisme maintient ce contrôle en équilibrant la production et la dégradation des hormones. Les boucles de rétroaction régissent l’amorce et le maintien de la plupart des sécrétions hormonales en réponse à divers stimuli.
Rôle des boucles de rétroaction
Faisons un bref survol de la contribution des boucles de rétroaction au maintien de l’homéostasie. Les boucles de rétroaction positive se caractérisent par la libération d’hormones supplémentaires en réponse à une libération initiale de ces mêmes hormones. La libération d’ocytocine pendant l’accouchement est un exemple de boucle de rétroaction positive. La libération initiale d’ocytocine indique aux muscles utérins de se contracter pour pousser le fœtus vers le col de l’utérus, ce qui a pour effet de dilater le col. Cette dilatation indique ensuite à l’hypophyse qu’elle doit libérer plus d’ocytocine, ce qui intensifie les contractions. Après la naissance de l’enfant, la libération d’ocytocine diminue.
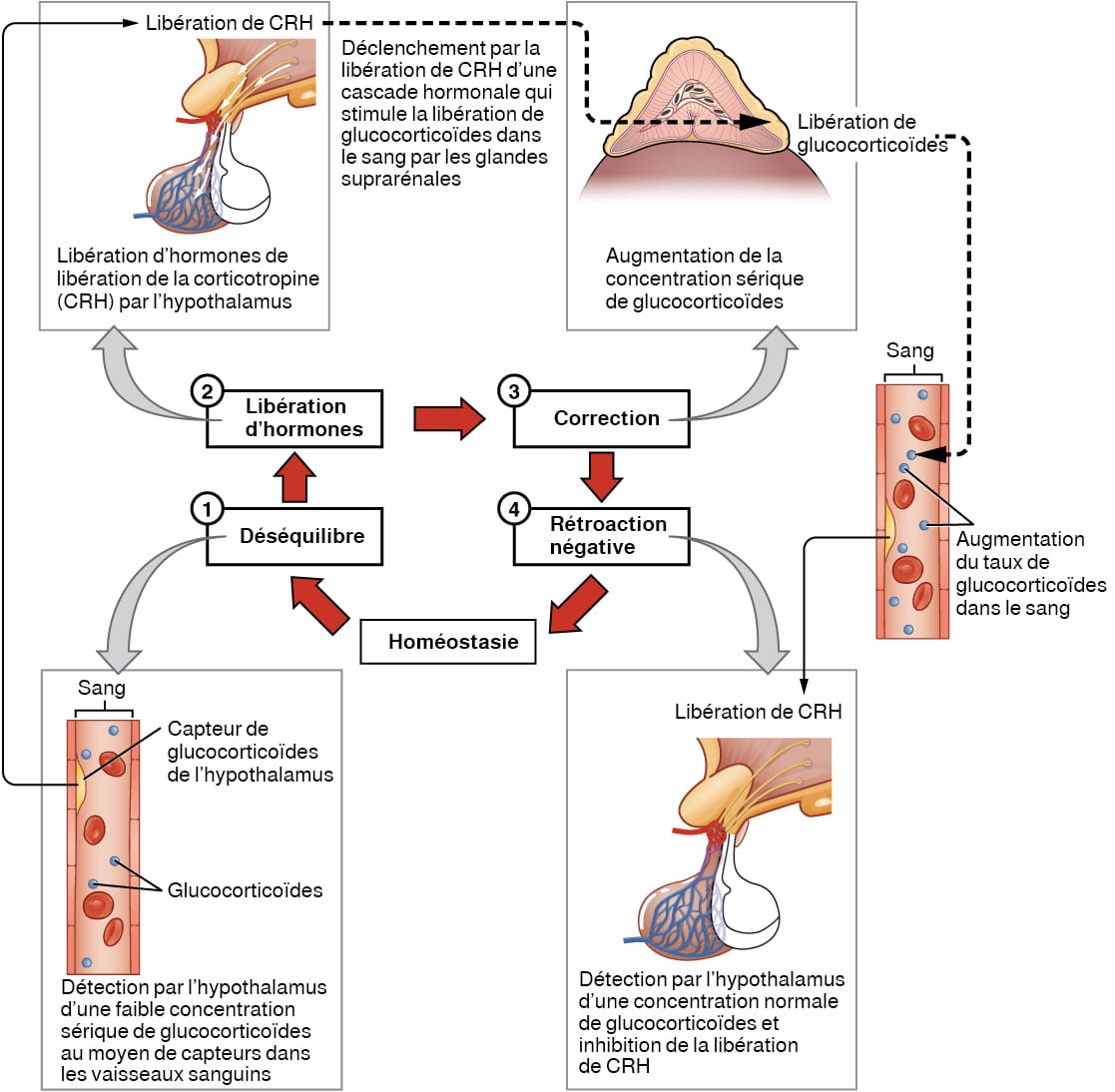
La boucle de rétroaction négative est toutefois la méthode de régulation hormonale la plus courante. La rétroaction négative se caractérise par l’inhibition de la sécrétion d’une hormone en réponse à un taux adéquat de cette hormone. Cette inhibition permet de maintenir le taux sérique d’une hormone dans une plage étroite de valeurs. La libération de glucocorticoïdes par les glandes suprarénales sous l’impulsion de l’hypothalamus et de l’hypophyse est un exemple de boucle de rétroaction négative. Au fur et à mesure que la concentration sérique de glucocorticoïdes augmente, l’hypothalamus et l’hypophyse réduisent le nombre de signaux qu’ils envoient aux glandes suprarénales afin d’empêcher qu’elles sécrètent d’autres glucocorticoïdes (voir la figure 20.3).
Hypophyse antérieure
L’hypophyse antérieure (aussi nommée « adénohypophyse » ou « antéhypophyse ») se forme à partir de la bouche primitive de l’embryon (aussi appelée « stomodaeum »), et migre vers le cerveau au fil du développement du fœtus. Elle se divise en trois régions : la partie distale (ou lobe antérieur), qui est la partie la plus en avant; la partie intermédiaire, adjacente au lobe postérieur de l’hypophyse (aussi appelé « neuro-hypophyse »); et la partie tubérale, un « tube » effilé qui enveloppe l’infundibulum.
Rappelons que l’hypophyse postérieure ne fait que stocker les hormones, elle ne les synthétise pas. En revanche, l’hypophyse antérieure en fabrique. La sécrétion hormonale de l’hypophyse antérieure est régulée par deux classes d’hormones sécrétées par l’hypothalamus : celles qui stimulent la sécrétion hormonale de l’hypophyse antérieure et celles qui l’inhibent.
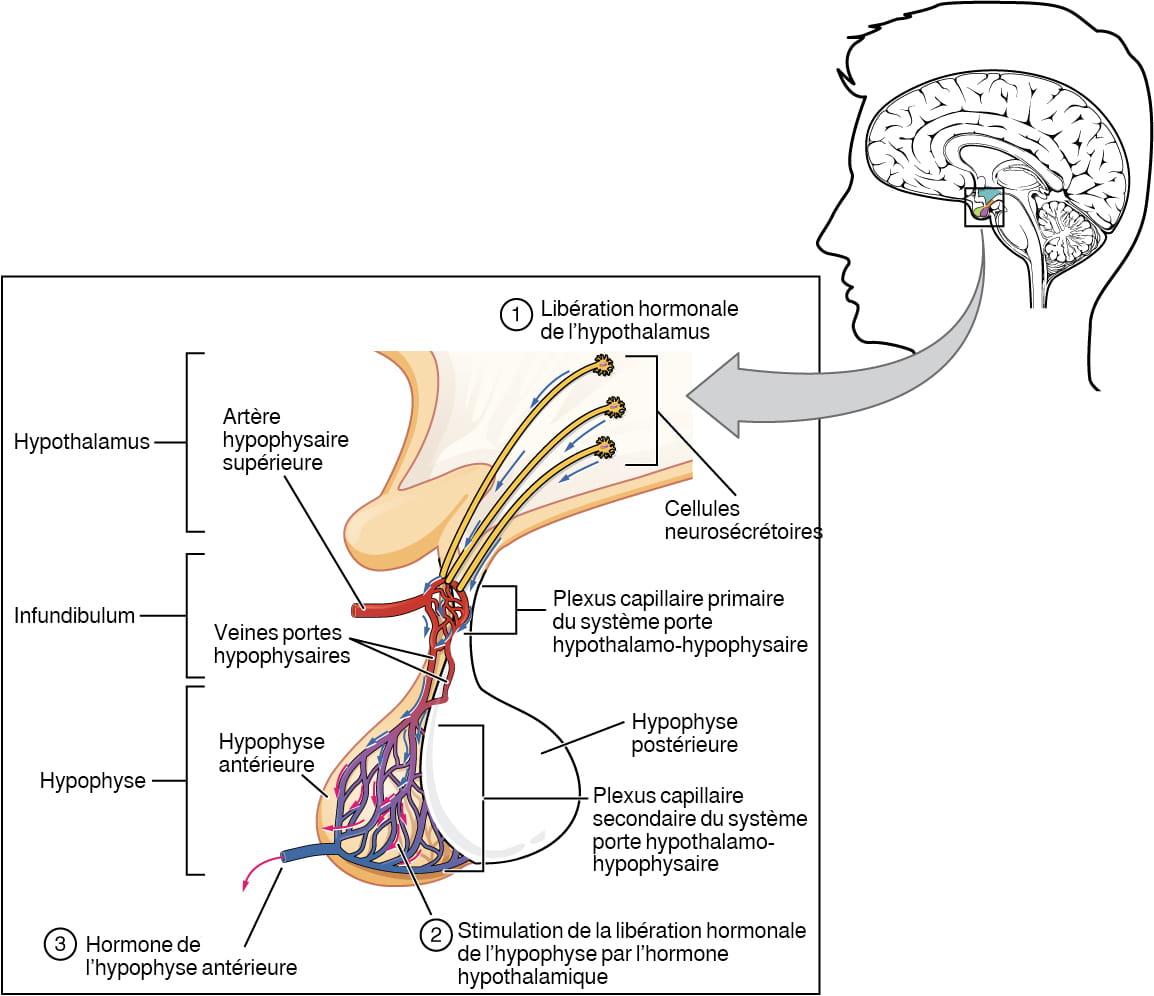
Les hormones hypothalamiques sont sécrétées par les neurones et pénètrent dans l’hypophyse antérieure par les vaisseaux sanguins. À l’intérieur de l’infundibulum se trouve un réseau de capillaires qui relient l’hypothalamus à l’hypophyse antérieure. Ce réseau appelé « système porte hypothalamo-hypophysaire » permet le transport des hormones hypothalamiques vers l’hypophyse sans qu’elles aient à passer dans la circulation systémique. Il commence dans l’artère hypophysaire supérieure, laquelle bifurque à partir des artères carotides et achemine le sang jusqu’à l’hypothalamus. Les branches de l’artère hypophysaire supérieure forment le système porte hypothalamo-hypophysaire (voir la figure 20.4). Les hormones de libération et d’inhibition en provenance de l’hypothalamus circulent par un plexus capillaire primaire jusqu’aux veines portes, puis sont transportées dans l’hypophyse antérieure. En réponse aux hormones de libération qu’elle reçoit, l’hypophyse antérieure produit des hormones qui suivent un plexus capillaire secondaire, puis se propagent dans la circulation sanguine.
L’hypophyse antérieure produit sept hormones : l’hormone de croissance (GH), la thyréostimuline (TSH), l’hormone adrénocorticotrope (ACTH), l’hormone folliculostimulante (FSH), l’hormone lutéinisante (LH), la bêta-endorphine et la prolactine. La TSH, l’ACTH, la FSH et la LH sont collectivement désignées comme des « hormones tropiques » (où « -trope » signifie « changer »), car elles activent ou désactivent les fonctions d’autres glandes endocrines.
Hormone de croissance
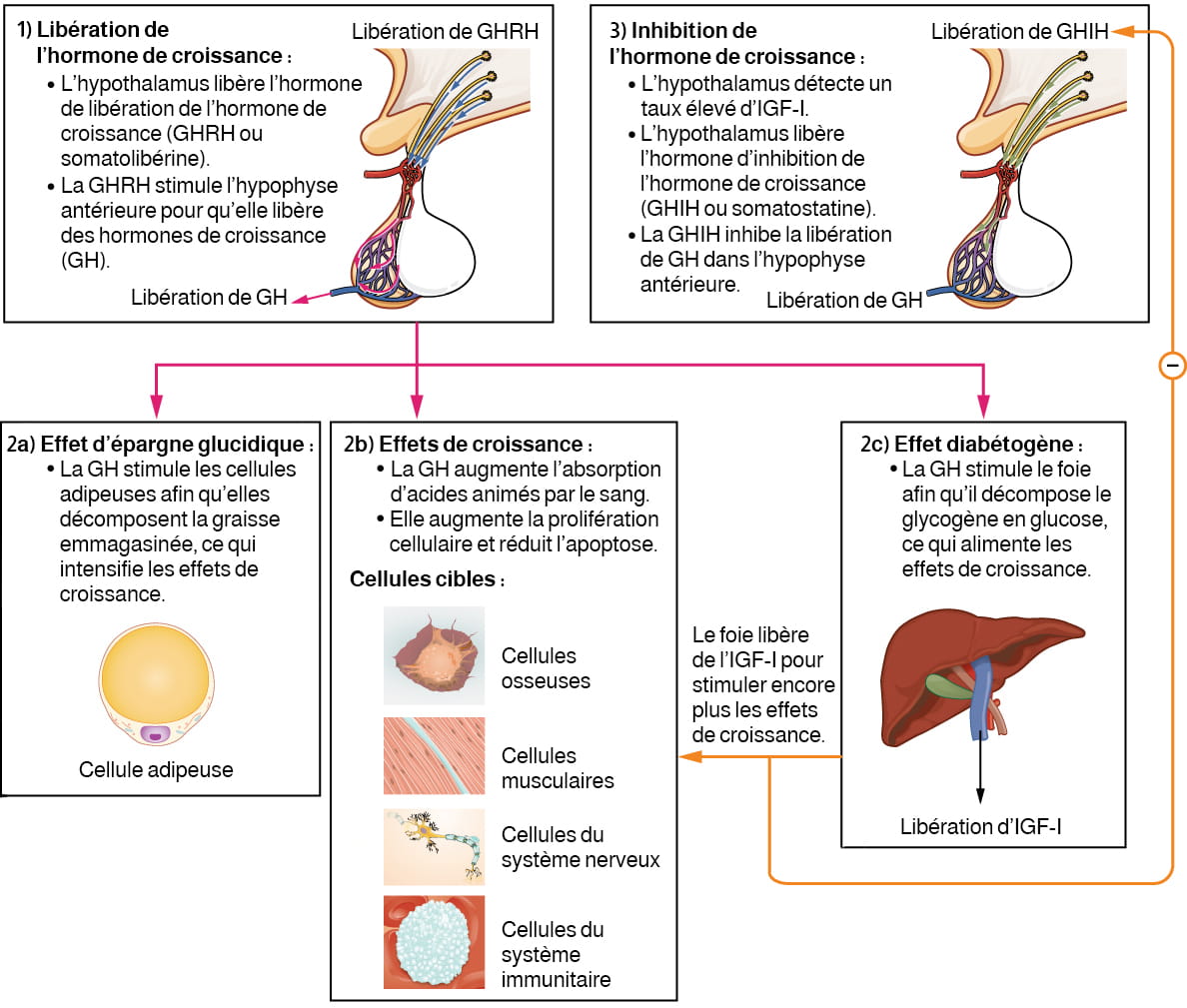
Le système endocrinien régule la réplication cellulaire, la synthèse des protéines et la croissance du corps humain. L’une des hormones qui contribuent principalement à ce processus est l’hormone de croissance (GH) (aussi appelée « somatotropine »), une hormone protéique produite et sécrétée par l’hypophyse antérieure. Sa fonction principale est anabolique, c’est-à-dire qu’elle favorise la synthèse des protéines et la formation de tissus (voir la figure 20.5). Le taux de GH est contrôlé par la libération par l’hypothalamus de l’hormone de libération de l’hormone de croissance (GHRH ou somatolibérine) et de la somatostatine (GHIH ou SRIH).
La GH stimule aussi la lipolyse, c’est-à-dire la dégradation des tissus adipeux. Ce phénomène libère des acides gras dans le sang, ce qui engendre un effet d’épargne glucidique. Concrètement, de nombreux tissus changent leur principale source d’énergie, passant du glucose aux acides gras. Ainsi, le glucose est prélevé du sang en moins grande quantité.
Le GH déclenche également l’effet diabétogène en stimulant le foie pour qu’il décompose le glycogène en glucose, lequel est ensuite déposé dans le sang. Le nom « diabétogène » provient du fait qu’un taux élevé de glucose dans le sang peut être observé autant chez les personnes souffrant de diabète sucré non traité que chez celles qui produisent de la GH en excès. L’effet d’épargne glucidique et l’effet diabétogène provoquent ensemble une augmentation de la glycémie.
La GH régule indirectement la croissance et la synthèse des protéines en incitant le foie et d’autres tissus à produire un groupe de protéines appelées les facteurs de croissance insulinomimétique (IGF). Ces protéines augmentent la prolifération cellulaire et inhibent l’apoptose, aussi appelée « mort cellulaire régulée ». Les IGF stimulent les cellules pour qu’elles absorbent plus d’acides aminés en provenance du sang afin d’effectuer la synthèse des protéines. Les cellules cartilagineuses et musculosquelettiques sont particulièrement sensibles à la stimulation des IGF.
Le dysfonctionnement du contrôle de la croissance par le système endocrinien peut entraîner plusieurs affections. Le gigantisme, par exemple, est une affection qui cause chez les enfants la sécrétion de quantités anormalement élevées de GH, ce qui entraîne une croissance excessive. L’acromégalie est une affection semblable qui survient chez les adultes et entraîne la croissance des os du visage, des mains et des pieds en réaction à un taux excessif de GH chez les personnes qui ont fini de grandir. Un taux anormalement faible de GH chez les enfants peut causer un déficit de croissance appelé « nanisme hypophysaire », ou déficit en hormone de croissance.
Hypophyse postérieure
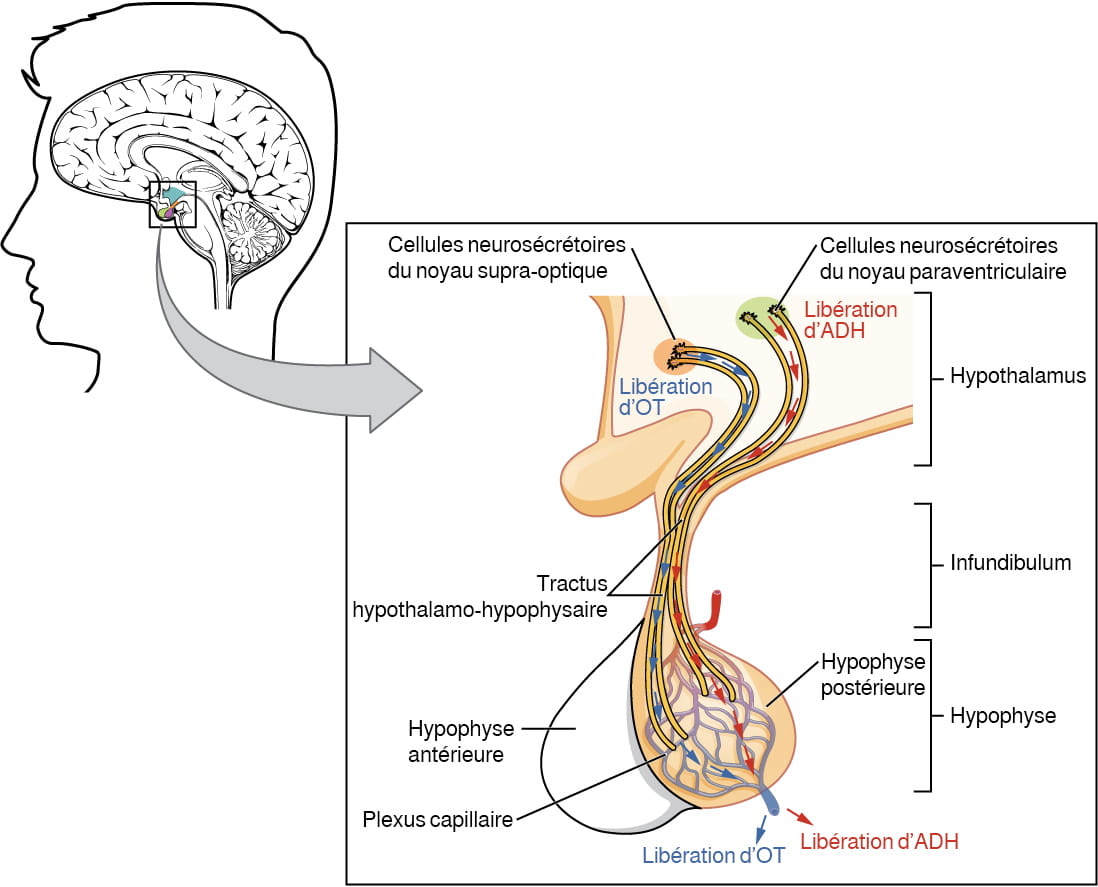
L’hypophyse postérieure (ou « neurohypophyse ») est en fait l’extension des neurones siégeant dans les noyaux de l’hypothalamus. Les corps cellulaires de ces régions se situent dans l’hypothalamus, mais leurs axones forment le tractus hypothalamo-hypophysaire à l’intérieur de l’infundibulum et se terminent par des terminaisons axonales qui constituent l’hypophyse postérieure (voir la figure 20.6).
L’hypophyse postérieure ne produit pas d’hormones, mais elle stocke et sécrète des hormones produites par l’hypothalamus. Les noyaux paraventriculaires produisent l’ocytocine et les noyaux supra-optiques produisent l’ADH. Ces hormones circulent dans les axones vers des sites de stockage dans les terminaisons axonales de l’hypophyse postérieure. Les hormones sont ensuite libérées dans le sang par les terminaisons axonales en réponse à ces mêmes neurones hypothalamiques.
Ocytocine
Une fois que le fœtus s’est complètement développé, l’hormone peptidique appelée « ocytocine » (où « -tocie » signifie « accouchement ») stimule les contractions utérines et la dilatation du col de l’utérus. Pendant la majeure partie de la grossesse, l’expression des récepteurs à l’ocytocine dans l’utérus est régulée à la baisse. Toutefois, vers la fin de la grossesse, la synthèse de ces récepteurs dans l’utérus augmente, ce qui augmente par le fait même la sensibilité des cellules musculaires lisses de l’utérus aux effets de l’ocytocine. L’ocytocine est libérée en continu tout au long de l’accouchement par une boucle de rétroaction positive. Comme mentionné précédemment, l’ocytocine déclenche les contractions utérines pour pousser la tête du fœtus vers le col de l’utérus. La dilatation du col stimule en retour la synthèse d’ocytocine supplémentaire par l’hypothalamus, puis sa libération par l’hypophyse, ce qui augmente l’intensité et l’efficacité des contractions et pousse le col à se dilater davantage. Cette boucle de rétroaction positive se poursuit jusqu’à la naissance du bébé.
Le saviez-vous?
L’ocytocine est utilisée pendant l’accouchement, mais aussi pendant l’allaitement.
Même si le taux élevé d’ocytocine dans le sang maternel diminue dès la naissance du bébé, l’hormone continue de contribuer à la santé de la mère et du nouveau-né. Tout d’abord, l’ocytocine est nécessaire au réflexe d’éjection du lait chez les femmes qui allaitent. Lorsque le nouveau-né commence à téter, les récepteurs sensoriels des mamelons transmettent des signaux à l’hypothalamus, ce qui déclenche en retour la sécrétion et la libération d’ocytocine dans le sang. En quelques secondes, les cellules des canaux lactifères maternels se contractent et éjectent le lait dans la bouche du nourrisson. Ensuite, l’ocytocine contribuerait, chez l’homme comme chez la femme, à tisser le lien entre parents et nourrisson, ce qu’on appelle « l’attachement ». On soupçonne aussi que l’ocytocine joue un rôle dans les sentiments d’amour et de proximité et dans la réponse sexuelle.
Hormone antidiurétique (ADH)
L’osmolarité sanguine, qui désigne la concentration d’un soluté dans le sang, peut varier en réponse à la consommation de certains aliments et liquides et en réponse aux maladies, blessures, médicaments ou autres facteurs. L’osmolarité du sang est contrôlée en permanence par les osmorécepteurs, des cellules spécialisées de l’hypothalamus particulièrement sensibles à la concentration d’ions sodium et autres solutés.
Lorsque l’osmolarité sanguine est élevée, ce qui peut survenir en cas de déshydratation ou après un repas très salé, les osmorécepteurs envoient des signaux à l’hypophyse postérieure pour qu’elle libère des hormones antidiurétiques (ADH). Les cellules cibles de l’ADH sont situées dans les cellules tubulaires rénales. Elles ont pour effet d’augmenter la perméabilité épithéliale à l’eau, accentuant ainsi la réabsorption de l’eau. La quantité d’eau réabsorbée par le filtrat glomérulaire est proportionnelle au volume d’eau qui sera réacheminé dans le sang, ce qui implique qu’une moins grande quantité d’eau sera alors excrétée dans l’urine. Ainsi, plus la concentration d’eau est importante, plus la concentration de solutés est réduite. L’ADH porte aussi le nom « vasopressine », car, à fortes concentrations, elle entraîne la constriction des vaisseaux sanguins, ce qui augmente la résistance vasculaire et, par la même occasion, la pression artérielle. La libération de l’ADH est régulée par une boucle de rétroaction négative. À mesure que l’osmolarité sanguine diminue, les osmorécepteurs hypothalamiques détectent la variation et déclenchent une diminution équivalente de la sécrétion d’ADH. Une moins grande quantité d’eau est alors réabsorbée par le filtrat glomérulaire.
Fait intéressant, les drogues peuvent avoir un effet sur la sécrétion d’ADH. Par exemple, la consommation d’alcool inhibe la libération d’ADH, ce qui augmente la production d’urine et peut éventuellement mener à la déshydratation et à la gueule de bois (ou « lendemain de veille »). Le diabète insipide est une maladie caractérisée par une sous-production chronique d’ADH qui entraîne une déshydratation chronique. La production et la sécrétion sous-optimales d’ADH font en sorte qu’une quantité insuffisante d’eau est réabsorbée par les reins. Même si les patients ressentent la soif et consomment plus de liquides, ils ne parviennent pas à diminuer efficacement la concentration de solutés dans leur sang, car leur taux d’ADH n’est pas assez élevé pour déclencher la réabsorption d’eau dans leurs reins. Plusieurs cas de diabète insipide peuvent donner lieu à des déséquilibres électrolytiques.
Thyréostimuline
L’activité de la glande thyroïde est régulée par la thyréostimuline (TSH ou thyrotropine). La TSH est libérée par l’hypophyse antérieure en réponse à l’hormone de libération de la thyréostimuline (TRH), sécrétée par l’hypothalamus. Elle active la sécrétion des hormones thyroïdiennes par la glande thyroïde. S’effectue alors une boucle de rétroaction négative classique : le taux élevé d’hormones thyroïdiennes dans le sang déclenche à son tour une chute de la production de TRH, puis de TSH.
Hormone adrénocorticotrope
L’hormone adrénocorticotrope (ACTH), aussi appelée « corticostimuline » ou « corticotropine », stimule les corticosurrénales (l’« écorce » à la surface des glandes suprarénales) pour qu’elles sécrètent des corticostéroïdes comme le cortisol. L’ACTH provient de la pro-opiomélanocortine (POMC), une molécule précurseur dont le clivage produit plusieurs molécules biologiquement actives, notamment l’ACTH, l’hormone α-mélanostimulante (α-MSH) et les neuropeptides opioïdes nommés « endorphines ». L’hypothalamus régule la libération de l’ACTH au moyen de l’hormone de libération de la corticotropine (CRH) en réponse aux rythmes physiologiques normaux. Divers facteurs de stress peuvent aussi influencer sa libération. Le rôle de l’ACTH dans la réponse au stress est abordé plus loin dans ce chapitre.
Hormone folliculostimulante et hormone lutéinisante
Les glandes endocrines, notamment l’hypophyse, les corticosurrénales et les gonades (ovaires et testicules), sécrètent plusieurs hormones qui contrôlent le développement et la régulation de l’appareil reproducteur. L’appareil reproducteur se développe majoritairement pendant la puberté, période où se développent les caractères sexuels spécifiques chez les adolescents et les adolescentes. La puberté est déclenchée par la gonadolibérine (GnRH), une hormone produite et sécrétée par l’hypothalamus. La GnRH stimule l’hypophyse antérieure afin qu’elle sécrète des gonadostimulines (ou « gonadotropines »), des hormones qui régulent le fonctionnement des gonades. Le taux de gonadolibérine est régulé par une boucle de rétroaction négative : un taux élevé d’hormones de reproduction inhibe la libération de GnRH. Les gonadostimulines régulent la fonction reproductive tout au long de la vie. Chez les femmes, elles régulent le début et la fin de la capacité de reproduction.
Les gonadolibérines comprennent deux glycoprotéines. La première, l’hormone folliculostimulante (FSH), stimule la production et la maturation des cellules sexuelles (gamètes), soit les ovules et les spermatozoïdes. Elle favorise aussi la croissance des follicules, lesquels libèrent ensuite des œstrogènes dans les ovaires. La deuxième, l’hormone lutéinisante (LH), déclenche l’ovulation ainsi que la production d’œstrogènes et de progestérone par les ovaires. Elle stimule aussi la production de testostérone par les testicules.
Prolactine
Comme son nom l’indique, la prolactine (PRL) favorise la lactation (production de lait) chez la femme. Elle contribue au développement des glandes mammaires pendant la grossesse et stimule la production de lait maternel par les glandes mammaires après l’accouchement. Les effets de la prolactine dépendent toutefois fortement des effets permissifs des œstrogènes, de la progestérone et d’autres hormones. Comme mentionné précédemment, le lait maternel est éjecté en réponse à la stimulation créée par l’ocytocine.
Chez les femmes non enceintes, la sécrétion de prolactine est inhibée par l’hormone inhibitrice de la libération de prolactine (PIH), qui s’avère être le neurotransmetteur appelé « dopamine » et qui est libérée par les neurones de l’hypothalamus. Le taux de prolactine augmente uniquement pendant la grossesse, en réponse à l’hormone de libération de la prolactine (PRH) sécrétée par l’hypothalamus.
Hypophyse intermédiaire : Hormone mélanostimulante
Les cellules contenues entre les lobes de l’hypophyse sécrètent des hormones mélanostimulantes (MSH), formées par le clivage d’une protéine précurseur appelée « pro-opiomélanocortine » (POMC). La production locale de MSH dans la peau régule la production de mélanine en réponse à l’exposition aux rayons UV. Le rôle de la MSH hypophysaire est toutefois plus complexe; par exemple, les personnes qui ont la peau claire ont généralement la même quantité de MSH que les personnes ayant une peau foncée. Néanmoins, la MSH a le pouvoir d’assombrir la peau en stimulant les mélanocytes de l’épiderme pour qu’ils produisent de la mélanine. Chez les femmes, la production de cette hormone augmente pendant la grossesse. Combinée aux œstrogènes, la MSH peut assombrir la pigmentation cutanée, en particulier dans la région des aréoles et des petites lèvres. Le tableau 20.4 présente un résumé sur les hormones hypophysaires et leurs principaux effets.
| ILLUSTRATIONS DES LOBES DE L’HYPOPHYSE | HORMONES | |||
|
Illustration présentant l’hypophyse postérieure
|
Hormones de l’hypophyse postérieure | |||
| Hormone de libération (hypothalamus) | Hormone hypophysaire | Cible | Effets | |
| ADH | Stockage de l’ADH | Reins, glandes sudoripares, système circulatoire | Maintient l’équilibre hydrique | |
| – | OT | Appareil reproducteur féminin | Déclenche les contractions utérines pendant l’accouchement | |
|
Illustration présentant l’hypophyse antérieure
|
Hormones de l’hypophyse antérieure | |||
| Hormone de libération (hypothalamus) | Hormone hypophysaire | Cible | Effets | |
| GnRH | LH | Appareil reproducteur | Stimule la production d’hormones sexuelles par les gonades | |
| GnRH | FSH | Appareil reproducteur | Stimule la production d’ovules et de spermatozoïdes | |
| TRH | TSH | Glande thyroïde | Stimule la libération d’hormones thyroïdiennes (TH), lesquelles régulent le métabolisme | |
| PRH (inhibée par la PIH) | PRL | Glandes mammaires | Favorise la production de lait maternel | |
| GHRH (inhibée par la GHIH) | GH | Foie, os, muscles | Incite les organes cibles à produire des facteurs de croissance insulinomimétique (IGF), lesquels stimulent la croissance et augmentent le taux métabolique | |
| CRH | ACTH | Glandes suprarénales | Incite les organes cibles à produire des glucocorticoïdes, lesquels régulent le métabolisme et la réponse au stress | |
Corps pinéal
Le corps pinéal est une minuscule glande endocrine dont les fonctions demeurent méconnues. Les pinéalocytes qui composent le corps pinéal produisent et sécrètent la mélatonine, une hormone amine dérivée de la sérotonine.
La sécrétion de mélatonine varie en fonction de l’intensité lumineuse que l’organisme reçoit de l’environnement. Lorsque les rétines sont stimulées par des photons de lumière, un influx nerveux est envoyé à la région de l’hypothalamus, qui joue un rôle essentiel dans la régulation des rythmes biologiques. Alors, le taux de mélatonine dans le sang diminue, ce qui favorise l’état d’éveil. À l’inverse, lorsque la luminosité diminue (p. ex., pendant la soirée), la production de mélatonine augmente, ce qui accentue sa présence dans le sang et provoque de la somnolence.
Regardez la vidéo :
La vidéo YouTube a été exclue de cette version du texte. Vous pouvez y accéder en ligne à l’adresse suivante : https://ecampusontario.pressbooks.pub/medicalterminology/?p=269.
Vidéo 20.2. What Does Melatonin Do? Melatonin Use Info (Quels sont les effets de la mélatonine? Renseignements sur son utilisation) [Vidéo en ligne]. © Travelers Defense, 2015.
Quelles actions diminuant le taux de mélatonine doit-on éviter de faire au milieu de son cycle de sommeil?
La sécrétion de mélatonine peut influencer les rythmes circadiens du corps, ces fluctuations entre l’obscurité et la luminosité qui influencent la somnolence et l’éveil, mais aussi l’appétit et la température corporelle. Fait intéressant, les enfants ont un taux plus élevé de mélatonine que les adultes, ce qui peut empêcher la libération de gonadolibérines par l’hypophyse antérieure et, par conséquent, inhiber l’amorce de la puberté. Enfin, des recherches actuelles se penchent sur un rôle antioxydant de la mélatonine.
Lorsqu’une personne traverse plusieurs fuseaux horaires, elle se sent somnolente le jour et éveillée la nuit : c’est l’effet du décalage horaire. Traverser ainsi plusieurs fuseaux horaires perturbe considérablement le cycle de lumière-obscurité régulé par la mélatonine. La synthèse de la mélatonine peut alors prendre jusqu’à plusieurs jours pour s’ajuster au cycle de lumière-obscurité du nouvel environnement, ce qui cause le décalage horaire. Lors de voyages en avion, certaines personnes prennent des suppléments de mélatonine pour s’endormir.
Glande thyroïde
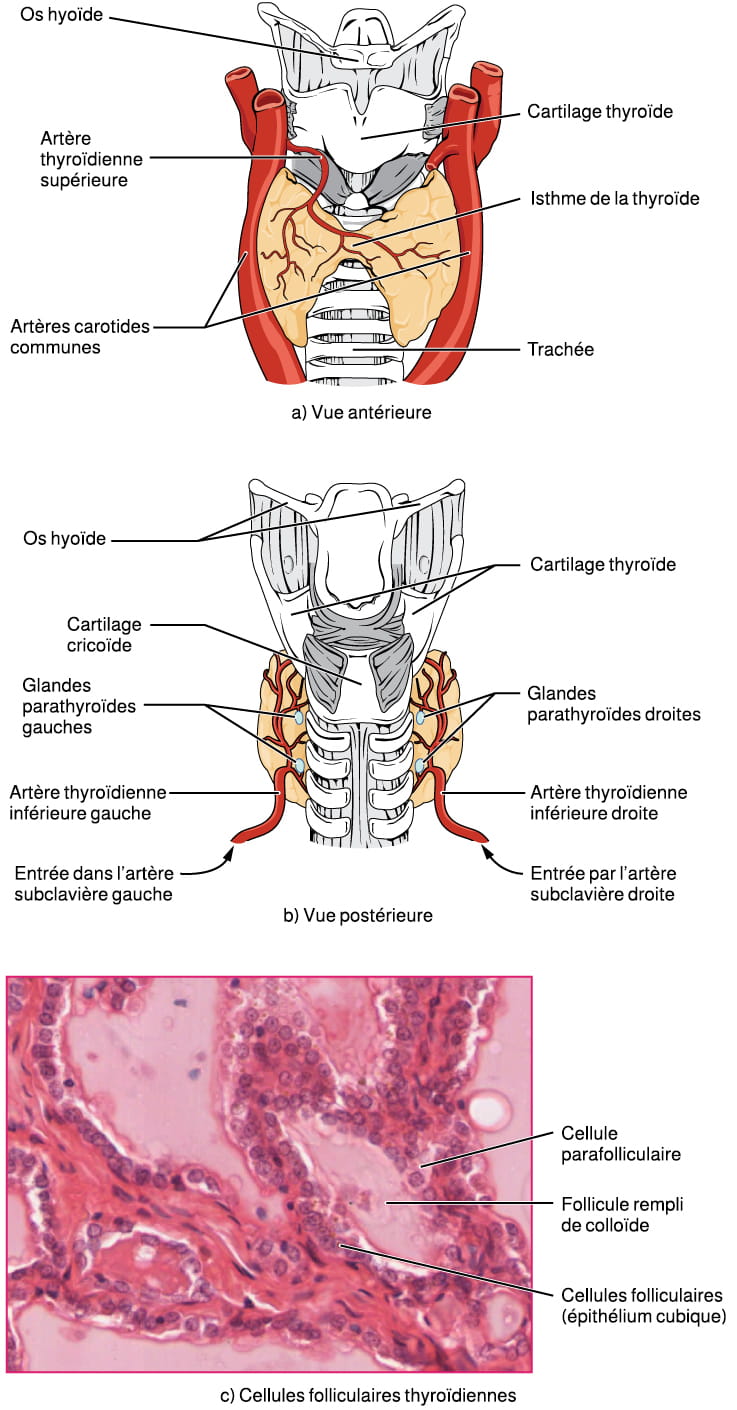
La glande thyroïde est un organe en forme de papillon situé devant la trachée et juste en dessous du larynx (voir la figure 20.7). Sa région médiane, appelée l’« isthme », est flanquée de lobes (gauche et droit) en forme d’ailes. Dans chacun des lobes sont incrustées deux glandes parathyroïdes, principalement sur la face postérieure. Le tissu de la glande thyroïde est majoritairement constitué de follicules thyroïdiens. Ces follicules sont formés d’une cavité centrale remplie d’un liquide visqueux appelé « colloïde ». Entouré d’une paroi de cellules folliculaires épithéliales, le colloïde est le centre de production des hormones thyroïdiennes; cette production hormonale dépend d’un composant unique et essentiel aux hormones : l’iode.
Régulation de la synthèse des hormones thyroïdiennes
La thyréostimuline (TSH) régule la libération de T3 et de T4 par la glande thyroïde. Un faible taux sérique de T3 et de T4 stimule l’hypothalamus pour qu’il libère l’hormone de libération de la thyréostimuline (TRH), qui déclenche la sécrétion de TSH par l’hypophyse antérieure. En retour, la TSH stimule la glande thyroïde pour qu’elle sécrète les hormones T3 et T4. Le taux de TRH, de TSH, de T3 et de T4 est régulé par une boucle de rétroaction négative dans laquelle l’augmentation du taux de T3 et de T4 fait diminuer la production et la sécrétion de TSH. Les hormones thyroïdiennes T3 et T4 sont souvent appelées « hormones métaboliques », car leur taux a une incidence sur le métabolisme basal, c’est-à-dire la quantité d’énergie utilisée par le corps au repos.
La glande thyroïde sécrète aussi la calcitonine, une hormone produite par les cellules parafolliculaires (cellules C) qui tapissent le tissu entre les follicules. La calcitonine est libérée en réponse à une augmentation du taux de calcium dans le sang.
Glandes parathyroïdes
Les glandes parathyroïdes sont de minuscules structures arrondies qui sont généralement incrustées dans la face postérieure de la glande thyroïde. Une épaisse capsule de tissu conjonctif sépare les parathyroïdes du tissu thyroïdien. La majorité des gens ont quatre glandes parathyroïdes, mais il arrive que d’autres soient présentes dans les tissus du cou ou de la poitrine. La fonction d’un type particulier de cellules parathyroïdiennes, les « cellules oxyphiles », demeure méconnue. Les cellules fonctionnelles primaires des glandes parathyroïdes sont les cellules principales. Ces cellules épithéliales produisent et sécrètent l’hormone parathyroïdienne (PTH ou parathormone), l’hormone principalement impliquée dans la régulation du taux de calcium dans le sang.
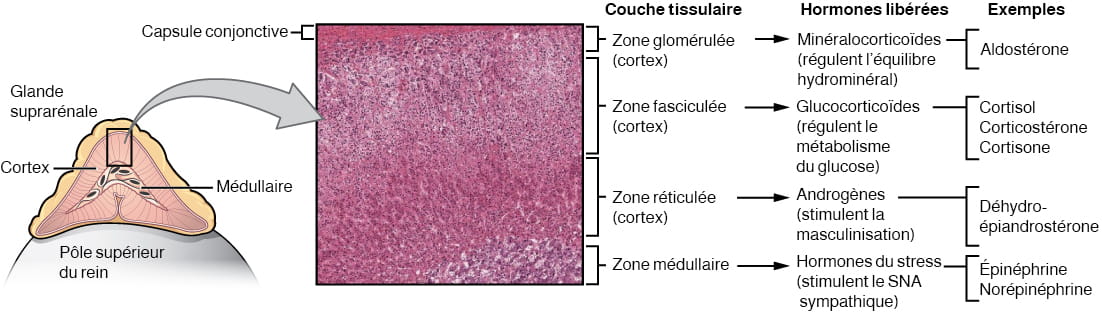
Glandes suprarénales
Les glandes suprarénales (ou glandes surrénales) sont des glandes neuroendocrines en forme de pyramide qui adhèrent au pôle supérieur de chaque rein par une capsule fibreuse (voir la figure 20.8). Les glandes suprarénales bénéficient d’un apport sanguin important et ont un débit sanguin parmi les plus élevés dans l’organisme. Elles sont irriguées par plusieurs branches collatérales de l’aorte, dont les artères suprarénales (ou capsulaires) et l’artère rénale. Le sang afflue vers chaque glande suprarénale par le cortex surrénal (aussi appelé « corticosurrénale ») et s’évacue par la médullaire de la glande suprarénale (ou « médullosurrénale »). Les hormones surrénaliennes sont libérées dans la circulation sanguine par les veines suprarénales gauche et droite.
En tant que composant de l’axe hypothalamo-hypophyso-surrénalien (HHS), la corticosurrénale sécrète des hormones stéroïdes essentielles à la régulation de la réponse au stress prolongé, de la pression artérielle, du volume sanguin, de l’absorption et du stockage des nutriments, de l’équilibre hydroélectrolytique et de l’inflammation. L’axe HHS joue un rôle dans la stimulation de l’hypophyse par l’hypothalamus pour qu’elle libère des hormones adrénocorticotropes (ACTH). L’ACTH stimule à son tour la corticosurrénale pour qu’elle produise du cortisol. Cette voie hormonale sera approfondie un peu plus loin.
La médullaire des glandes suprarénales est composée de tissu neuroendocrine constitué de neurones postganglionnaires du système nerveux sympathique (SNS). Autrement dit, c’est une extension du système nerveux autonome, qui régule l’homéostasie dans le corps. La voie sympatho-surrénalienne-médullaire (SSM) se définit par la stimulation de la zone médullaire des glandes suprarénales par des influx nerveux envoyés par l’hypothalamus via les neurones de la moelle épinière dorsale. Cette stimulation déclenche la sécrétion des amines épinéphrine et norépinéphrine par la zone médullaire.
La réponse au stress est l’une des principales fonctions des glandes suprarénales. Le stress peut prendre une forme purement physique ou psychologique ou être une combinaison des deux. La malnutrition et l’exposition du corps à des blessures ou à des températures extérieures froides et humides sans protection sont des exemples de stress physiques. Les stress psychologiques peuvent comprendre la perception d’une menace physique, une dispute avec un être cher ou simplement une mauvaise journée à l’école.
L’organisme répond de multiples façons au stress de courte et de longue durée, selon un comportement qu’on appelle « syndrome général d’adaptation » (SGA). La première phase du SGA est la réaction d’alarme. Il s’agit de la réaction de lutte ou de fuite, un stress de courte durée régulé par l’épinéphrine et la norépinéphrine, des hormones sécrétées par la médullaire des glandes suprarénales et acheminées par la voie SSM. Elles ont pour fonction de préparer le corps à un effort physique extrême. Le corps revient rapidement à la normale une fois ce type de stress éliminé. Cette réponse au stress est abordée plus en détail dans la section sur la médullaire des glandes suprarénales.
Si le stress n’est pas rapidement soulagé, le corps s’adapte au stress lors de la deuxième phase : la phase de résistance. Par exemple, si une personne est affamée, son corps pourrait envoyer des signaux au tube digestif pour qu’il maximise l’absorption des nutriments contenus dans les aliments.
Toutefois, si le stress se prolonge, le corps répond par l’apparition de symptômes bien différents de la réaction de lutte ou de fuite. À la phase d’épuisement, une personne peut commencer à souffrir de dépression ou de fatigue extrême, connaître une suppression de sa réponse immunitaire, ou même mourir d’une crise cardiaque. Ces symptômes sont régulés par les hormones corticosurrénaliennes, en particulier le cortisol, dont la libération est déclenchée par des signaux envoyés via l’axe HHS.
Les hormones surrénaliennes ont aussi plusieurs fonctions qui ne sont pas liées au stress, comme l’augmentation du taux de sodium et de glucose dans le sang qui sera approfondie plus loin.
Corticosurrénale
La corticosurrénale est constituée de plusieurs couches de cellules riches en réserves lipidiques organisées en trois régions structurellement distinctes. Chaque région produit différentes hormones.
Regardez la vidéo :
Vidéo 20.3. Endocrine System, Part 2 – Hormone Cascades: Crash Course A&P #24 (Système endocrinien, partie 2 – Cascades hormonales : cours accéléré en anatomie et physiologie no 24) [Vidéo en ligne]. © CrashCourse, 2015.
Vérification des connaissances
- Quelle hormone produite par les glandes suprarénales est responsable de mobiliser les réserves énergétiques?
Hormones de la zone glomérulée
La région la plus superficielle de la corticosurrénale est appelée « zone glomérulée ». Elle produit un groupe d’hormones collectivement appelées « minéralocorticoïdes », qui doivent leur nom à l’effet qu’elles ont sur les minéraux dans l’organisme, en particulier le sodium et le potassium. Ces hormones sont essentielles pour maintenir l’équilibre hydroélectrolytique du corps.
L’aldostérone est le minéralocorticoïde le plus important; elle joue un rôle essentiel dans la régulation des concentrations d’ions sodium (Na+) et potassium (K+) dans l’urine, la sueur et la salive. Par exemple, en réponse à un taux sérique élevé de K+, à un faible taux sérique de Na+, à une pression artérielle faible ou à un faible volume sanguin, l’aldostérone est libérée pour augmenter l’excrétion de K+ et la rétention de Na+, ce qui a pour effet d’augmenter le volume sanguin et la pression artérielle. La sécrétion de l’aldostérone s’amorce lorsque la CRH hypothalamique déclenche la libération d’ACTH par l’hypophyse antérieure.
L’aldostérone est également un composant essentiel du système régine-angiotensine-aldostérone (SRAA), dans lequel des cellules rénales spécialisées sécrètent l’enzyme appelée « rénine » en réponse à une pression artérielle ou un volume sanguin faibles. La rénine catalyse la conversion de l’angiotensinogène, une protéine sanguine produite par le foie, en l’hormone angiotensine I. L’enzyme de conversion de l’angiotensine (ECA) convertit ensuite l’angiotensine I en angiotensine II dans les poumons. L’angiotensine II a trois principales fonctions :
- Amorcer une vasoconstriction des artérioles pour diminuer le débit sanguin.
- Stimuler les tubules rénaux afin qu’ils réabsorbent de l’eau et du chlorure de sodium (NaCl) pour augmenter le volume sanguin.
- Envoyer des signaux à la corticosurrénale afin qu’elle sécrète de l’aldostérone, dont les effets contribuent à la rétention hydrique et rétablissent la pression artérielle et le volume sanguin.
Des médicaments qui inhibent la production d’angiotensine II sont offerts aux personnes qui souffrent d’hypertension artérielle. Appelés « inhibiteurs de l’enzyme de conversion de l’angiotensine » (IECA), ces médicaments empêchent l’ECA de convertir l’angiotensine I en angiotensine II, atténuant ainsi sa capacité à augmenter la pression artérielle.
Hormones de la zone fasciculée
La région intermédiaire de la corticosurrénale est la « zone fasciculée », ainsi nommée parce que les cellules qui la composent forment de petits « fascicules » (ou amas) séparés par de minuscules vaisseaux sanguins. Les cellules de la zone fasciculée produisent les glucocorticoïdes, des hormones impliquées dans le métabolisme du glucose. La plus importante de ces hormones est le cortisol, dont une certaine partie est convertie en cortisone par le foie. La corticostérone est un autre glucocorticoïde produit en beaucoup plus faible quantité. En réponse à des facteurs de stress prolongé, l’hypothalamus sécrète de la CRH, qui déclenche en retour la libération d’ACTH par l’hypophyse antérieure. L’ACTH déclenche ensuite la libération des glucocorticoïdes. L’effet global de ces hormones est d’inhiber la formation de tissus tout en stimulant la dégradation des nutriments emmagasinés afin de maintenir des réserves énergétiques adéquates. Par exemple, face à une situation de stress prolongé, le cortisol favorise le catabolisme du glycogène en glucose, des triglycérides stockés en glycérol et en acides gras, et des protéines musculaires en acides aminés. Ces matières premières peuvent ensuite être utilisées pour la synthèse de glucose et de cétones supplémentaires pouvant servir de carburant pour l’organisme. L’hippocampe, qui fait partie du lobe temporal du cortex cérébral et qui est essentiel à la formation de la mémoire, est extrêmement sensible au stress puisqu’il possède de nombreux récepteurs aux glucocorticoïdes.
Vous connaissez sûrement les médicaments sur ordonnance ou en vente libre qui contiennent des glucocorticoïdes, par exemple : les injections de cortisone dans les articulations enflammées; les comprimés de prednisone et les inhalateurs (pompes) à base de stéroïdes pour la prise en charge de l’asthme sévère; et les crèmes à l’hydrocortisone appliquées pour soulager les démangeaisons provoquées par des éruptions cutanées. Ces médicaments témoignent d’un autre rôle du cortisol, soit la régulation négative du système immunitaire, qui inhibe la réponse inflammatoire.
Hormones de la zone réticulée
La région la plus profonde de la corticosurrénale est la « zone réticulée ». Elle produit en petites quantités une classe d’hormones sexuelles stéroïdes appelées « androgènes ». Les androgènes sont produits dans les gonades durant la puberté et la majeure partie de la vie adulte. Les androgènes produits dans la zone réticulée servent à compléter les androgènes gonadiques. Leur production est déclenchée par la libération d’ACTH par l’hypophyse antérieure et ils sont ensuite convertis en testostérone ou en œstrogènes dans les tissus. Les androgènes peuvent contribuer à la libido chez la femme adulte, mais leur fonction chez l’homme adulte n’est pas encore bien comprise. Chez les femmes ménopausées, à mesure que la fonction ovarienne diminue, les androgènes produits par la zone réticulée deviennent la principale source d’œstrogènes.
Médullaire des glandes suprarénales
Comme mentionné précédemment, la corticosurrénale libère des glucocorticoïdes en réponse à un stress prolongé, comme une maladie grave. À l’inverse, la médullaire des glandes suprarénales libère ses hormones en réponse à un stress intense de courte durée, régulé par le système nerveux sympathique (SNS).
Le tissu médullaire est constitué de neurones postganglionnaires uniques assimilables au SNS : les chromaffines. Ces larges cellules de forme irrégulière produisent l’épinéphrine (ou adrénaline) et la norépinéphrine (ou noradrénaline), deux neurotransmetteurs. L’épinéphrine, produite en plus grande quantité (selon un ratio d’environ 4 pour 1), est plus puissante que la norépinéphrine. Puisqu’elles sont libérées dans la circulation sanguine par les chromaffines, où elles se propagent ensuite largement pour exercer leurs effets sur des cellules éloignées, l’épinéphrine et la norépinéphrine sont considérées comme des hormones. Dérivées de l’acide aminé « tyrosine », elles appartiennent à la classe chimique des catécholamines.
La sécrétion médullaire d’épinéphrine et de norépinéphrine est régulée par une voie neuronale qui prend naissance dans l’hypothalamus en réponse à un danger ou un stress (la voie SSM). Les deux catécholamines envoient des signaux aux cellules hépatiques et musculosquelettiques afin qu’elles convertissent le glycogène en glucose pour augmenter la glycémie. Ces hormones augmentent la fréquence cardiaque, le pouls et la pression artérielle afin de préparer le corps à lutter contre la menace qu’il perçoit ou à la fuir. De plus, la voie SSM dilate les voies respiratoires et les vaisseaux sanguins, ce qui augmente le taux d’oxygène dans le sang, et par conséquent, l’oxygénation d’organes essentiels tels que les poumons, le cerveau, le cœur et les muscles squelettiques. Elle déclenche en même temps la vasoconstriction de vaisseaux sanguins qui irriguent des organes moins essentiels tels que le tube digestif, les reins et la peau, et assure la régulation négative de certains composants du système immunitaire. La voie SSM provoque aussi d’autres effets comme la sécheresse buccale, la perte d’appétit, la dilatation des pupilles et la perte de la vision périphérique.
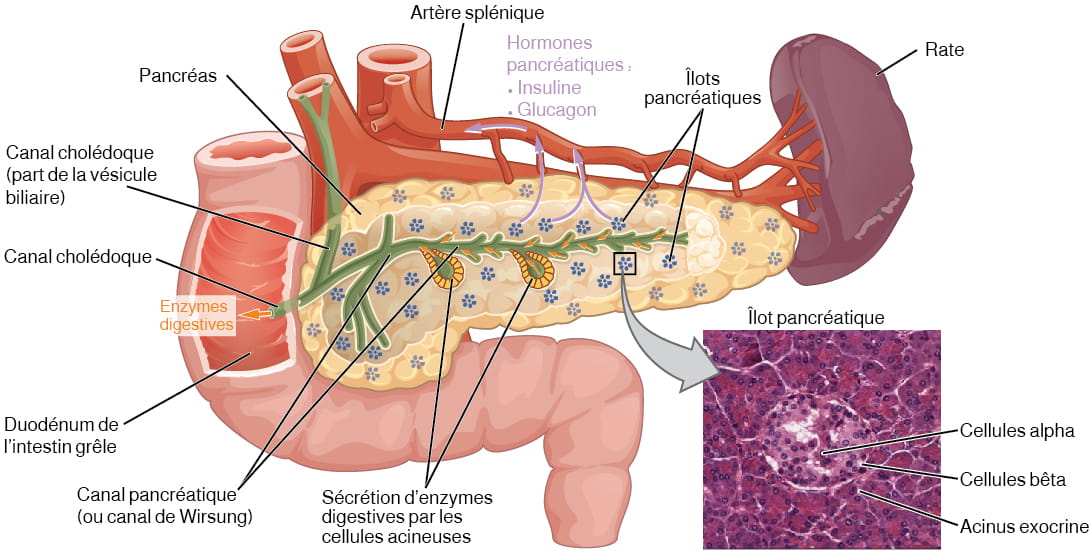
Pancréas
Le pancréas est un organe long et mince situé en majeure partie derrière la moitié inférieure de l’estomac (voir la figure 20.9). Bien qu’il soit principalement une glande exocrine qui sécrète diverses enzymes digestives, le pancréas a aussi une fonction endocrine. Ses îlots pancréatiques (des amas de cellules anciennement appelés « îlots de Langerhans ») sécrètent différentes hormones : le glucagon, l’insuline, la somatostatine et le polypeptide pancréatique (PP).
Cellules et sécrétions des îlots pancréatiques
Chaque îlot pancréatique contient quatre types de cellules :
- Les cellules alpha (α) produisent le glucagon et constituent environ 20 % de chaque îlot. Le glucagon est libéré en réponse à un faible taux de glucose dans le sang. Il joue un rôle important dans la régulation de la glycémie.
- Les cellules bêta (β) produisent l’insuline et constituent environ 75 % de chaque îlot. L’insuline est libérée en réponse à un taux élevé de glucose dans le sang.
- Les cellules delta (δ) constituent 4 % des cellules de chaque îlot et sécrètent la somatostatine. Rappelons que cette hormone peptidique est également libérée par l’hypothalamus (sous la forme de GHIH) et est aussi sécrétée par l’estomac et les intestins. La somatostatine pancréatique est une hormone inhibitrice de la libération du glucagon et de l’insuline.
- Les cellules PP constituent environ 1 % des cellules de chaque îlot et sécrètent le polypeptide pancréatique. Cette hormone jouerait un rôle dans l’appétit et la régulation des sécrétions pancréatiques endocrines et exocrines. Le polypeptide pancréatique peut être libéré après un repas pour diminuer la consommation subséquente de nourriture, mais il est aussi libéré en réponse au jeûne.
Régulation de la glycémie par l’insuline et le glucagon
Le glucose est nécessaire à la respiration cellulaire et constitue la source d’énergie préférée par l’ensemble des cellules de l’organisme. Le corps tire le glucose de la dégradation des aliments et boissons riches en glucides que nous consommons. Le glucose qui n’est pas immédiatement utilisé comme carburant par les cellules peut être stocké sous forme de glycogène par le foie et les muscles ou converti en triglycérides puis stocké dans les tissus adipeux. Les hormones régulent le stockage et l’utilisation du glucose en fonction des besoins. Des récepteurs situés dans le pancréas détectent le taux de glycémie et les cellules pancréatiques sécrètent ensuite du glucagon ou de l’insuline pour maintenir un taux normal de glucose dans le sang.
Glandes gonadiques
Les glandes gonadiques désignent les ovaires et les testicules, qui produisent les cellules sexuelles (ovules et spermatozoïdes) et sécrètent les hormones gonadiques. Les rôles des gonadolibérines libérées par l’hypophyse antérieure (FSH et LH) ont déjà été abordés.
La testostérone est l’hormone principale produite par les testicules. Cette hormone stéroïde est essentielle à la maturation des cellules spermatozoïdes et au développement de l’appareil reproducteur masculin et des caractères sexuels secondaires masculins, comme la voix grave, la pilosité et l’augmentation de la masse musculaire. Fait intéressant, la testostérone est aussi produite dans les ovaires, quoiqu’en bien plus petite quantité. Les testicules produisent aussi l’inhibine, une hormone peptidique qui inhibe la sécrétion de FSH par l’hypophyse antérieure. La FSH stimule la spermatogenèse.
Les ovaires produisent principalement des œstrogènes, notamment l’estradiol, l’œstriol et l’œstrone (ou folliculine). Les œstrogènes jouent un rôle important dans de nombreux processus physiologiques, notamment : la régulation du cycle menstruel, le maintien de la grossesse, et le développement du tissu mammaire, de l’appareil reproducteur féminin et des caractères sexuels secondaires féminins, comme l’augmentation de la quantité de tissus adipeux. La progestérone est une autre hormone ovarienne importante; elle contribue à réguler le cycle menstruel et est essentielle pour préparer le corps à la grossesse et maintenir la grossesse. En outre, les cellules de la granulosa des follicules ovariens produisent de l’inhibine, qui, comme chez l’homme, inhibe la sécrétion de FSH. Au début de la grossesse, le placenta se développe dans l’utérus. Cet organe fournit au fœtus un apport en oxygène et en nutriments, évacue les déchets dans la circulation maternelle et produit et sécrète des œstrogènes et de la progestérone. Le placenta produit aussi la gonadotrophine chorionique (hCG), qui favorise la synthèse de la progestérone et diminue la fonction immunitaire maternelle afin de protéger le fœtus d’un rejet immunologique. Il sécrète également l’hormone placentaire lactogène (hPL), qui contribue à la préparation des seins à la lactation, et la relaxine, qui aiderait à ramollir et à élargir la symphyse pubienne en vue de l’accouchement.
Abréviations courantes du système endocrinien Un élément interactif ou multimédia a été exclu de cette version du texte. Vous pouvez y accéder en ligne à l’adresse suivante :
https://ecampusontario.pressbooks.pub/medicalterminology/?p=269.
Vérification des connaissances
- Vous rappelez-vous quel terme désigne un taux élevé de glucose dans le sang?
- Vous rappelez-vous quel neurotransmetteur contribue à la réponse au danger ou au stress?
- D’après vous, que se passerait-il si la corticosurrénale ne réussissait pas à sécréter ses hormones?
Maladies et troubles
Acromégalie
- Trouble chez l’adulte qui survient lorsqu’un taux anormalement élevé de GH déclenche une croissance excessive des mains, des pieds et des os du visage.
Maladie d’Addison
Maladie rare qui engendre un faible taux de sodium dans le sang et une hypoglycémie. Les signes et symptômes de la maladie d’Addison sont nébuleux et caractéristiques d’autres maladies, ce qui en complique le diagnostic. Ils peuvent comprendre une faiblesse généralisée, des douleurs abdominales, une perte de poids, des nausées, des vomissements, des sueurs et un goût accru pour des aliments salés (Betts et coll., 2013).
Syndrome de Cushing
Maladie caractérisée par une hyperglycémie et par l’accumulation de dépôts lipidiques sur le cou et le visage. Elle est causée par une hypersécrétion de cortisol. Le syndrome de Cushing est le plus souvent dû à la présence d’une tumeur hypophysaire qui sécrète du cortisol ou de l’ACTH en quantités anormalement élevées; on parle alors de « maladie de Cushing » (Betts et coll., 2013).
Gigantisme
- Trouble chez l’enfant qui survient lorsqu’un taux anormalement élevé de GH déclenche une croissance excessive du corps (Betts et coll., 2013).
Hirsutisme
Symptôme d’une production excessive d’androgènes entraînant chez les femmes l’apparition de poils à des endroits où il n’y en a pas habituellement. Bien qu’une production accrue d’androgènes puisse être attribuable à certains médicaments, elle peut aussi être liée à des troubles endocriniens comme le syndrome des ovaires polykystiques (SOPK), le syndrome de Cushing et les tumeurs ovariennes ou surrénaliennes (Mayo Clinic, 2020).
Hyperthyroïdie
Affection caractérisée par un taux élevé d’hormones thyroïdiennes entraînant une perte de poids, une transpiration abondante et une augmentation de la fréquence cardiaque (Betts et coll., 2013).
Hypothyroïdie
Affection caractérisée par un faible taux d’hormones thyroïdiennes entraînant un gain de poids, une sensibilité accrue au froid et un ralentissement de l’activité mentale (Betts et coll., 2013).
Maladie de Basedow
Affection caractérisée par un trouble de la glande thyroïde qui entraîne une hyperthyroïdie (Betts et coll., 2013).
Diabète insipide
Maladie causée par un manque ou une hyposécrétion d’hormones antidiurétiques (ADH). Le diabète insipide peut aussi être causé par l’incapacité des reins à répondre à l’ADH (Betts et coll., 2013).
Diabète (ou diabète sucré)
Maladie caractérisée par un trouble pancréatique qui entraîne une hyperglycémie (Betts et coll., 2013).
Termes médicaux en contexte
Un élément interactif ou multimédia a été exclu de cette version du texte. Vous pouvez y accéder en ligne à l’adresse suivante :
https://ecampusontario.pressbooks.pub/medicalterminology/?p=269.
Un élément interactif ou multimédia a été exclu de cette version du texte. Vous pouvez y accéder en ligne à l’adresse suivante :
https://ecampusontario.pressbooks.pub/medicalterminology/?p=269.
Spécialités médicales et interventions associées au système endocrinien
L’endocrinologie est une spécialisation du domaine médical qui s’intéresse surtout au traitement des troubles du système endocrinien. Les endocrinologues, des médecins spécialisés dans ce domaine, sont des experts dans le traitement des maladies associées aux systèmes hormonaux, des maladies thyroïdiennes au diabète. Les spécialistes en chirurgie endocrinienne traitent les maladies endocriniennes par l’ablation de la glande ou du tissu endocrine. Certaines personnes éprouvent des problèmes de santé causés par la baisse normale de production d’hormones qui vient avec l’âge. Elles peuvent consulter un.e endocrinologue pour soupeser les risques et avantages d’un traitement hormonal substitutif, destiné à stimuler leur taux naturel d’hormones de reproduction. En plus de traiter les patient.e.s, les endocrinologues peuvent mener des recherches pour contribuer à une meilleure compréhension des troubles du système endocrinien et mettre au point de nouveaux traitements pour guérir ces maladies (Betts et coll., 2013).
- Les spécialistes de la thyroïde sont des endocrinologues surspécialisés dans le traitement des troubles de la glande thyroïde, comme l’hypothyroïdie (hyposécrétion) et l’hyperthyroïdie (hypersécrétion).
- Les diabétologues sont des endocrinologues surspécialisés dans le traitement du diabète.
Interventions
Scintigraphie de la thyroïde
Technique d’imagerie visant à vérifier l’état de la glande thyroïde. La scintigraphie de la thyroïde consiste à administrer et situer un composé radioactif dans la glande thyroïde (Giorgi et Cherney, 2018). Pour en savoir plus sur la scintigraphie de la thyroïde, consulter le site HealthLine: Thyroid Scan.
Absorption d’iodes radioactifs
Méthode d’évaluation de la fonction thyroïdienne qui consiste à injecter des iodes radioactifs, puis à mesurer la quantité d’iodes éliminés du sang par la glande thyroïde (MedlinePlus, 2020). Pour en savoir plus sur le test d’absorption d’iodes radioactifs, consulter le site Medline Plus: Radioactive Iodine Uptake.
Dosage sérique
Analyse sanguine visant à déterminer la concentration et la présence de diverses hormones endocrines dans le sang. Le dosage sérique permet entre autres d’évaluer le taux de calcium, de cortisol, d’électrolytes, de FSH, de GH, de glucose, d’insuline, d’hormones parathyroïdiennes, de T3, de T4, de TSH et de testostérone dans le sérum sanguin (Betts et coll., 2013).
Interventions en chirurgie endocrinienne
La plupart des interventions chirurgicales touchant le système endocrinien impliquent l’ablation ou l’incision d’une glande. Lorsqu’on excise une glande endocrine en raison d’une tumeur ou d’une hypertrophie, il faut prescrire un traitement hormonal substitutif. En effet, des médicaments sont nécessaires pour remplacer de manière artificielle ou synthétique l’hormone produite par la glande et la fonction qu’elle régule (Betts et coll., 2013).
Lexique sur le système endocrinien
- Autocrine
Signal chimique qui suscite une réponse dans la cellule même qui l’a sécrété.
Glande endocrine
Tissu ou organe exempt de conduit excréteur qui sécrète des hormones dans le sang et la lymphe de sorte qu’elles puissent circuler loin du site de sécrétion.
Système endocrinien
Ensemble de cellules, de tissus et d’organes dont la fonction primaire ou secondaire est la sécrétion hormonale, et qui jouent un rôle intégral dans les processus normaux de l’organisme.
Épinéphrine
Hormone et neurotransmetteur, aussi appelée « adrénaline », produite par les glandes suprarénales.
Système exocrine
Cellules, tissus et organes qui sécrètent des substances directement vers les tissus cibles par des conduits excréteurs.
Histamine
Amine qui participe à la réponse inflammatoire et qui provoque généralement des démangeaisons.
Hormone
Sécrétion d’un organe endocrine qui circule par la circulation sanguine ou lymphatique pour provoquer une réponse dans des tissus ou cellules cibles ailleurs dans le corps.
Neurotransmetteur
Substance chimique qui joue le rôle de molécule de signalisation permettant la neurotransmission.
Norépinéphrine
Substance chimique naturellement présente dans l’organisme qui agit à la fois comme hormone du stress et comme neurotransmetteur (substance qui envoie des signaux entre les cellules nerveuses). Elle est libérée comme hormone de stress dans le sang lorsque le cerveau perçoit un stress.
Paracrine
Signal chimique qui suscite une réponse dans les cellules adjacentes à celle qui l’a sécrété; aussi appelé « facteur paracrine ».
Perméabilité
Propriété d’une membrane de laisser passer des liquides ou des gaz.
Prolifération
Multiplication rapide.
Synthèse
Formation d’un composé chimique par une réaction obtenue par la combinaison de corps simples ou de composés moins complexes.
Mettez vos connaissances à l’épreuve!
Un élément interactif ou multimédia a été exclu de cette version du texte. Vous pouvez y accéder en ligne à l’adresse suivante :
https://ecampusontario.pressbooks.pub/medicalterminology/?p=269.
Références
CrashCourse. (22 juin 2015). Endocrine system, part 1 – Glands & hormones: Crash course A&P #23 [Vidéo]. YouTube. https://www.youtube.com/watch?v=eWHH9je2zG4
CrashCourse. (29 juin 2015). Endocrine system, part 2 – Hormone cascade: Crash course A&P #24 [Vidéo]. YouTube. https://youtu.be/SCV_m91mN-Q
Giorgi, A. et Cherney, K. (2018). Thyroid scan. Healthline. https://www.healthline.com/health/thyroid-scan
MedlinePlus. (2020). Radioactive iodine uptake. US National Library of Medicine. https://medlineplus.gov/ency/article/003689.htm
Shurkin, J. N. (2 août 2013). Trouble sleeping? Go camping: Artificial light sources can negatively affect circadian rhythms, scientists say. Scientific American. https://www.scientificamerican.com/article/trouble-sleeping-go-campi/
TravelersDefense. (28 juillet 2009). What does melatonin do? Melatonin use info [Vidéo]. YouTube. https://www.youtube.com/watch?v=EUyBDGgsk_I
Description des images
Description de la figure 20.1 : Sur cette photo, une fillette étire le bras pour attraper une feuille orange tombant d’un chêne. Elle se trouve sur une passerelle près d’un ruisseau. La rive opposée s’étire en une pente raide couverte d’autres arbres aux couleurs d’automne. [Retour à la figure 20.1]
Description de la figure 20.2 : Ce diagramme illustre les glandes et cellules endocrines de l’ensemble du corps. Les organes du système endocrinien comprennent le corps pinéal et l’hypophyse, situés dans le cerveau. L’hypophyse se situe sur la face antérieure du thalamus et le corps pinéal, sur sa face postérieure. La thyroïde est une glande en forme de papillon qui enveloppe une partie de la trachée, dans la gorge. Quatre petites glandes en forme de disque, appelées « parathyroïdes », sont insérées dans la face postérieure de la thyroïde. Les glandes suprarénales se situent sur le pôle supérieur de chaque rein. Le pancréas se situe au centre de l’abdomen. Chez la femme, les deux ovaires sont reliés à l’utérus par deux longs tubes recourbés (trompes de Fallope) dans la région pelvienne. Chez l’homme, les deux testicules se trouvent dans le scrotum, sous le pénis. [Retour à la figure 20.2]
Description de la figure 20.3 : Ce diagramme illustre une boucle de rétroaction négative en utilisant comme exemple la régulation des glucocorticoïdes dans le sang. La première étape du cycle illustre l’apparition d’un déséquilibre. L’hypothalamus détecte une faible concentration de glucocorticoïdes dans le sang, visible par le peu de glucocorticoïdes (5) qui flottent dans la coupe transversale d’une artère. La deuxième étape du cycle est la libération hormonale, où l’hypothalamus libère l’hormone de libération de la corticotropine (CRH). La troisième étape est la correction. À cette étape, la libération de CRH déclenche une cascade hormonale qui stimule les glandes suprarénales pour qu’elles libèrent des glucocorticoïdes dans le sang. La concentration sérique de glucocorticoïdes s’en trouve ainsi augmentée, comme illustré par la présence de 8 molécules de glucocorticoïdes dans la coupe transversale de l’artère. La quatrième étape est la boucle de rétroaction négative, où l’hypothalamus détecte une concentration normale de glucocorticoïdes dans le sang et cesse la libération de CRH. Le taux sérique de glucocorticoïdes retrouve ainsi son équilibre (homéostasie). [Retour à la figure 20.3]
Description de la figure 20.4 : Cette illustration présente un gros plan de l’hypothalamus et de l’hypophyse qui s’y fixe. L’hypophyse antérieure est mise en évidence. Trois cellules neurosécrétoires sécrètent des hormones vers un réseau capillaire rappelant un filet, à l’intérieur de l’infundibulum. Ce filet capillaire porte le nom de « plexus capillaire primaire du système porte hypothalamo-hypophysaire ». L’artère hypophysaire supérieure rejoint le plexus capillaire primaire à partir de l’extérieur de l’infundibulum. Les veines portes hypophysaires descendent du plexus capillaire primaire, traversent l’infundibulum et se joignent au plexus capillaire secondaire du système porte hypothalamo-hypophysaire. Le plexus capillaire secondaire se trouve dans l’hypophyse antérieure. Les hormones libérées par les cellules neurosécrétoires de l’hypothalamus traversent le plexus capillaire primaire, descendent dans les veines portes hypophysaires, puis entrent dans le plexus capillaire secondaire. Rendues à destination, les hormones hypothalamiques stimulent alors l’hypophyse antérieure pour qu’elle libère ses hormones. Les hormones de l’hypophyse antérieure quittent le plexus capillaire secondaire par une veine unique située au bas du lobe hypophysaire antérieur. [Retour à la figure 20.4]
Description de la figure 20.5 : Cet organigramme illustre la cascade hormonale qui stimule la croissance humaine. À la première étape, l’hypothalamus libère l’hormone de libération de l’hormone de croissance (GHRH). La GHRH traverse le plexus capillaire primaire jusqu’à l’hypophyse antérieure, puis stimule l’hypophyse pour qu’elle libère l’hormone de croissance (GH). La libération de la GH entraîne trois types d’effets. L’effet d’épargne glucidique : la GH stimule les cellules adipeuses pour qu’elles décomposent la graisse emmagasinée, ce qui alimente l’effet de croissance (deuxième effet, abordé ci-dessous). Les cellules ciblées par l’effet d’épargne glucidique sont les cellules adipeuses. L’effet de croissance : la GH augmente l’absorption d’acides aminés par le sang et amplifie la prolifération cellulaire tout en diminuant l’apoptose. Les cellules ciblées par l’effet de croissance sont les cellules osseuses, musculaires, nerveuses et immunitaires. L’effet diabétogène : la GH stimule le foie pour qu’il décompose le glycogène en glucose, ce qui alimente l’effet de croissance. Le foie libère également des IGF en réponse à la GH. Les IGF stimulent l’effet de croissance, mais envoient aussi à l’hypothalamus des signaux de rétroaction négative. Lorsque l’hypothalamus détecte un taux élevé d’IGF-I, il libère l’hormone d’inhibition de l’hormone de croissance (GHIH). La GHIH inhibe la libération de GH par l’hypophyse antérieure. [Retour à la figure 20.5]
Description de la figure 20.6 : Cette illustration présente un gros plan de l’hypothalamus et de l’hypophyse qui s’y fixe. L’hypophyse postérieure est mise en évidence. Dans l’hypothalamus se trouvent deux noyaux contenant des cellules neurosécrétoires qui libèrent différentes hormones. Les cellules neurosécrétoires du noyau paraventriculaire libèrent l’ocytocine (OT) et celles du noyau supra-optique libèrent l’hormone antidiurétique (ADH). Les cellules neurosécrétoires s’étirent le long de l’infundibulum jusque dans l’hypophyse postérieure. Les prolongements tubulaires des cellules neurosécrétoires à l’intérieur de l’infundibulum sont collectivement appelés le « tractus hypothalamo-hypophysaire ». Ce tractus rejoint dans l’hypophyse postérieure un réseau de vaisseaux sanguins rappelant un filet, ce qu’on appelle le « plexus capillaire ». Stimulée par les signaux qu’elle reçoit par le plexus capillaire, l’hypophyse postérieure sécrète ensuite l’OT ou l’ADH dans une veine unique qui sort de l’hypophyse. [Retour à la figure 20.6]
Description de la figure 20.7 : La partie A de cette figure présente une illustration de la vue antérieure de la glande thyroïde. La thyroïde est une glande en forme de papillon qui enveloppe une partie de la trachée. Elle rétrécit en son centre, juste en dessous du cartilage thyroïde du larynx. Cette zone étroite est ce qu’on appelle l’« isthme de la thyroïde ». Deux grosses artères appelées les « artères carotides communes » longent la thyroïde parallèlement à la trachée. Une petite artère pénètre la surface supérieure de la thyroïde, près de l’isthme, et se ramifie pour traverser les deux « ailes » de la glande. La partie B de cette figure présente une vue postérieure de la thyroïde. On peut y voir que la thyroïde n’enveloppe pas complètement la partie postérieure de la trachée. Les faces postérieures des « ailes » de la thyroïde sont visibles sous le cartilage cricoïde du larynx. Chacune contient deux petites glandes en forme de disque appelées « parathyroïdes », qui sont insérées dans le tissu thyroïdien. Les disques sont disposés l’un au-dessus de l’autre dans chaque « aile ». On les appelle les glandes parathyroïdes gauches et droites. Juste en dessous des glandes parathyroïdes inférieures se trouvent deux artères qui irriguent la thyroïde à partir des artères subclavières gauche et droite. La partie C de cette figure représente une photomicrographie du tissu thyroïdien. Les cellules folliculaires thyroïdiennes sont des cellules épithéliales cubiques. Elles forment un anneau autour de cavités de forme irrégulière appelées « follicules ». Les follicules contiennent du colloïde, une substance de couleur claire. Une cellule parafolliculaire, plus grosse, est insérée entre deux cellules folliculaires près du pourtour d’un follicule. [Retour à la figure 20.7]
Description de la figure 20.8 : Ce diagramme illustre la glande suprarénale gauche, située sur le pôle supérieur du rein gauche. Cette glande est constituée d’une partie externe (cortex) et d’une partie interne (médullaire), le tout enveloppé d’une capsule conjonctive. Le cortex peut être subdivisé en d’autres zones, qui produisent toutes différents types d’hormones. La couche la plus en surface se nomme la « zone glomérulée » : elle libère les minéralocorticoïdes, comme l’aldostérone, qui régulent l’équilibre hydrominéral. Sous cette couche se trouve la zone fasciculée : elle libère les glucocorticoïdes, comme le cortisol, la corticostérone et la cortisone, qui régulent le métabolisme du glucose. La couche en dessous se nomme la « zone réticulée » : elle libère les androgènes, comme la déhydroépiandrostérone, qui stimulent la masculinisation (ou virilisation). La couche la plus profonde est la zone médullaire de la glande suprarénale : elle libère les hormones du stress, comme l’épinéphrine et la norépinéphrine, qui stimulent le système nerveux autonome (SNA) sympathique. [Retour à la figure 20.8]
Description de la figure 20.9 : Cette illustration montre l’anatomie du pancréas. La partie gauche du pancréas, plus volumineuse, repose dans la courbe du duodénum de l’intestin grêle. La partie droite, plus petite, est située près de la rate. On peut voir l’artère splénique qui traverse le pancréas jusqu’à la rate, mais qui se ramifie en plusieurs branches reliées au pancréas. Une vue interne du pancréas montre le canal pancréatique (ou canal de Wirsung), un gros tube qui traverse le centre du pancréas. Il se ramifie sur toute la longueur de l’organe en plusieurs acini en forme de fer à cheval contenant des cellules acineuses. Ces cellules sécrètent les enzymes digestives, qui circulent le long du canal cholédoque jusque dans l’intestin grêle. On peut aussi voir de petits îlots pancréatiques disséminés dans tout le pancréas. Les îlots pancréatiques sécrètent dans l’artère splénique les hormones pancréatiques appelées « insuline » et « glucagon ». Une photomicrographie montre que les îlots pancréatiques sont de petits disques de tissu composés d’un mince anneau externe appelé « acinus exocrine », d’un anneau interne plus épais de cellules bêta et d’un cercle central de cellules alpha. [Retour à la figure 20.9]
Sauf indication contraire, le chapitre présente du contenu adapté du manuel Anatomy and Physiology (sur OpenStax), de Betts et coll., et est utilisé sous la licence internationale CC BY 4.0. Téléchargez ou consultez gratuitement le manuel à l’adresse openstax.org/books/anatomy-and-physiology/pages/1-introduction.